Glukokortikoide, eine Gruppe von Hormonen, die unter anderem zur Behandlung von Allergien, rheumatischen und Autoimmunerkrankungen eingesetzt werden, sind auch während der Schwangerschaft von Bedeutung. Ihre Anwendung erfordert jedoch besondere Vorsicht, da Entwicklungsstörungen beim Ungeborenen drohen können. Die körpereigenen Glukokortikoide, wie das in der Nebennierenrinde produzierte Cortisol, sind essenziell für die Regulierung des Stoffwechsels und der Immunantwort sowie für die Entwicklung von Organen wie Gehirn und Lunge. Diese Hormone werden als Reaktion auf Stress freigesetzt und können von der Mutter auf den Fötus übertragen werden.
Die Wirkstoffe der Glukokortikoide sind vom körpereigenen Cortisol abgeleitet und besitzen entzündungshemmende, immunsuppressive und antiallergische Eigenschaften. Sie unterliegen zudem dem zirkadianen Rhythmus, mit maximaler Produktion in den Morgenstunden und minimaler Produktion in der Nacht. Glukokortikoide sind in verschiedenen Formen erhältlich, darunter zur oralen, dermalen und inhalativen Therapie.
Auswirkungen von Glukokortikoiden auf die fetale Gehirnentwicklung
Forschende haben untersucht, wie Stresshormone die frühe Entwicklung von Gehirnzellen in der Großhirnrinde von Föten beeinflussen. Die Hirnrinde ist ein entscheidender Bereich des Gehirns für das Denken. In einer Studie stellten Forschende fest, dass Glukokortikoide, wenn sie früh in der Schwangerschaft, im ersten oder frühen zweiten Trimester, verabreicht werden, die Anzahl eines bestimmten Typs von Gehirnzellen erhöhen können: die sogenannten basalen Vorläuferzellen. Diese Zellen werden sehr früh in der Entwicklung gebildet und sind wichtig für das Wachstum der Großhirnrinde.
Für ihre Untersuchungen verwendeten die Wissenschaftlerinnen und Wissenschaftler sogenannte Gehirnorganoide. Dies sind Modelle des sich entwickelnden Gehirns, die aus menschlichen Haut- oder Blutzellen gewonnen und in einer Petrischale kultiviert werden. Sie bilden frühe Entwicklungsstadien des heranreifenden Gehirns nach und ermöglichen Einblicke in die ersten Schritte der Gehirnentstehung.
Glukokortikoide wirken über ein Protein namens ZBTB16 auf die Entwicklung der Hirnrinde ein, was zur verstärkten Produktion von Nervenzellen führt. Eine genetische Variante, die als Reaktion auf Glukokortikoide zu einem Anstieg des ZBTB16-Spiegels führt, wurde mit einem kausalen Zusammenhang zwischen einer veränderten Gehirnstruktur und einem höheren Bildungsniveau im späteren Leben in Verbindung gebracht.
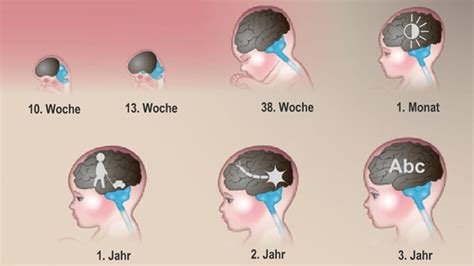
Unterschiedliche Auswirkungen je nach Schwangerschaftsphase
In der Vergangenheit haben viele Studien gezeigt, dass Glukokortikoide, wenn sie spät in der Schwangerschaft, im dritten Trimester, eingenommen werden, negative Auswirkungen auf die Nachkommen haben können. Dazu gehören der Verlust neuronaler Verbindungen und ein erhöhtes Risiko für psychiatrische Störungen im späteren Leben. Dies hängt mit der Neurogenese zusammen, dem Prozess der Bildung von Nervenzellen aus Vorläuferzellen, der in der frühen, aber nicht in der späten Schwangerschaft aktiv ist.
Im Gegensatz dazu haben die neueren Forschungen ergeben, dass Glukokortikoide in der frühen Schwangerschaft die Anzahl der Vorläuferzellen und Neuronen erhöhen können, was mit potenziell vorteilhaften Auswirkungen für die Nachkommen, wie zum Beispiel verbesserten kognitiven Fähigkeiten, einhergehen könnte.
Potenzielle Risiken und Nutzen von Glukokortikoiden in der Schwangerschaft
Die Gabe von Glukokortikoiden bei werdenden Müttern kann potenziell psychische und neurologische Störungen bei Kindern zur Folge haben. Eine Studie, die die Daten von mehr als einer Million Kindern analysierte, die zwischen 1996 und 2016 geboren wurden, hat diesen Verdacht bestätigt. Forschende verglichen die Entwicklung von Kindern, deren Mütter während der Schwangerschaft mit Glukokortikoiden behandelt wurden, mit der von Kindern ohne pränatale Exposition. Gründe für die Behandlung waren entweder eine Autoimmun- oder entzündliche Erkrankung oder das Risiko einer Frühgeburt.
Ein möglicher Grund für die Beeinträchtigung der Hirnentwicklung liegt darin, dass die systemische Gabe von Glukokortikoiden bei Schwangeren dazu führen kann, dass die Wirkstoffe in den Kreislauf des Babys gelangen und so die Hirnentwicklung beeinträchtigen. Dies kann zur Entstehung psychischer und neurologischer Störungen beitragen.
Glukokortikoide
Spezifische Risiken im ersten Trimester
Im ersten Trimester der Schwangerschaft besteht ein erhöhtes Risiko für die Entwicklung einer Lippen-Kiefer-Gaumenspalte (LKG) nach einer Therapie mit systemischen Glukokortikoiden. Obwohl die Studienlage hierzu nicht abschließend ist, gibt es Hinweise aus Tierversuchen und einigen Fall-Kontrollstudien beim Menschen, die auf ein solches erhöhtes Risiko hindeuten. Kleinere prospektive Kohortenstudien mit über 1000 exponierten Schwangerschaften und retrospektive Studien mit über 2500 exponierten Schwangerschaften konnten jedoch kein erhöhtes Risiko für LKG oder spezifische Fehlbildungen feststellen.
Weitere potenzielle Auswirkungen
Abhängig von Therapiedauer, Dosis und Indikation kann es nach systemischer Anwendung von Prednisolon vermehrt zu Frühgeburtlichkeit und einem geringeren Geburtsgewicht kommen. Diese Effekte sind jedoch oft schwierig von den Auswirkungen der zugrundeliegenden mütterlichen Erkrankung abzugrenzen. In einer Studie mit über 500 Rheumapatientinnen stieg das Risiko für Frühgeburten nach einer Langzeittherapie mit 10 mg/Tag Prednisolon-Äquivalentdosis oder mehr signifikant an.
Ob eine pränatale Glukokortikoid-Exposition vermehrt zu postnatalen Infektionen führt oder diese reduziert, wie bei der Lungenreifeinduktion, ist Gegenstand der Diskussion. Die bisherige Studienlage erlaubt keine abschließende Beurteilung, inwieweit ein Gestationsdiabetes oder eine Präeklampsie durch eine systemische Glukokortikoidtherapie in der Schwangerschaft gefördert werden.
Neonatale Anpassungsstörungen wie Hypoglykämien oder Elektrolytverschiebungen können nach einer Glukokortikoidtherapie in der Spätschwangerschaft auftreten.
Individuelle Nutzen-Risiko-Abwägung und Anwendungsrichtlinien
Eine systemische oder lokale Behandlung mit Prednisolon darf nach einer individuellen Risiko-Nutzen-Abwägung in allen Phasen der Schwangerschaft durchgeführt werden. Bei einer selten erforderlichen hohen systemischen Prednisolon-Therapie über Wochen sollte das fetale Wachstum sonographisch kontrolliert werden.
Prednisolon ist ein nicht-fluoriertes Glucocorticoid. Es ist die biologisch aktive Form des Prednisons und beeinflusst dosisabhängig den Stoffwechsel fast aller Gewebe. Prednisolon besitzt nur eine geringe mineralocorticoide Wirkung. Es wird in der Plazenta durch die 11β-Hydroxysteroid-Dehydrogenase enzymatisch inaktiviert, so dass vergleichsweise wenig Prednisolon den Fetus erreicht (in etwa 10-13%). Es kann oral, intravenös, rektal und lokal (intraartikulär, Auge, Ohr, Haut und Schleimhäute) angewendet werden.
Die Forschenden plädieren daher für einen umsichtigen Einsatz von Glukokortikoiden wie Cortison bei Schwangeren. Gleichzeitig betonen sie, dass der Verzicht auf die jeweiligen Wirkstoffe bei entsprechenden Erkrankungen ebenfalls schwere Folgen haben kann. Daher sollte stets eine sorgfältige Nutzen-Risiko-Analyse durchgeführt werden. Dies wird auch in den Fachinformationen einiger Glucocorticoid-haltiger Präparate empfohlen.
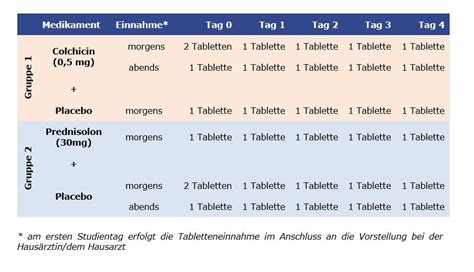
Glukokortikoide und Stillzeit
Für den gestillten Säugling ergibt sich selbst durch eine kurzdauernde Hochdosisbehandlung kein Risiko, da er über die Muttermilch nur einen Bruchteil einer üblicherweise gut verträglichen therapeutischen Kinderdosis erhält. Prednisolon, Prednison und Methylprednisolon sind Glukokortikoide der Wahl für eine systemische Behandlung während der Stillzeit. Auch hohe Dosen bis 1 g, einmalig oder wenige Tage nacheinander verabreicht, z.B. beim Asthmaanfall oder bei multipler Sklerose, erfordern keine Einschränkung des Stillens. Bei wiederholter Gabe solch hoher Dosen sollte, wenn es sich einrichten lässt, drei bis vier Stunden mit dem Stillen gewartet werden. Eine lokale Prednisolon-Therapie ist für den gestillten Säugling unbedenklich.
Die Rolle von Stresshormonen in der Schwangerschaft
Das endogene Glucocorticoid Cortisol spielt bei der normalen fetalen (Gehirn-)Entwicklung eine Rolle. Werden Glukokortikoide der Mutter jedoch systemisch und in hohen Mengen gegeben, könnte zu viel Glucocorticoid in den Kreislauf des Fetus gelangen. Kleinere Studien hatten eine systemische Anwendung von Corticosteroiden bei Müttern mit psychischen beziehungsweise neurologischen Störungen der Kinder in Verbindung gebracht. Diese Studien hatten jedoch methodische Mängel.
Forschende der Universität Zürich haben in Zusammenarbeit mit dem Universitätsspital Zürich und dem Max-Planck-Institut München herausgefunden, dass psychischer Stress der Mutter den Stoffwechsel in der Plazenta verändern und auch das Wachstum des Ungeborenen beeinflussen kann. Bei Stress schüttet der menschliche Körper Hormone aus, um mit der höheren Belastung umzugehen: so etwa das sogenannte Corticotropin-Releasing-Hormon (CRH), das in der Folge das Stresshormon Cortisol ansteigen lässt. Dieser Mechanismus bleibt auch in der Schwangerschaft bestehen, und die Plazenta kann das Stresshormon CRH ebenfalls freisetzen. Dadurch gelangt es in kleiner Menge in den fetalen Kreislauf und ins Fruchtwasser.
Aus Tierstudien ist bekannt, dass dieses Hormon die Entwicklung der Ungeborenen ankurbeln kann. Es wird verstärkt ausgeschüttet, wenn die Wachstumsbedingungen im Mutterleib ungünstig sind, um die Überlebenschancen angesichts einer zu frühen Geburt zu erhöhen. Unter Umständen kann dies auch negative Folgen haben: „Wird das Wachstum zu sehr beschleunigt, kann dies auf Kosten einer ausdifferenzierten Reifung der Organe geschehen", so Studienleiterin und Psychologin Ulrike Ehlert.
Das Forschungsteam untersuchte 34 gesunde Schwangere, die sich einer Fruchtwasserpunktion unterzogen. Eine solche Untersuchung stellt eine Belastungssituation für die werdenden Mütter dar, ihr Körper schüttet kurzfristig Cortisol aus. Um festzustellen, ob auch die Plazenta Stresshormone freisetzt, verglichen die Forschenden den Cortisol-Spiegel im mütterlichen Speichel mit dem CRH-Spiegel im Fruchtwasser - und stellten keinen Zusammenhang fest. „Offenbar bleibt das Baby bei akuter, kurzanhaltender Belastung der Mutter vor den negativen Effekten von Stress geschützt", folgert Psychologin Ulrike Ehlert.
Ganz anders die Resultate bei anhaltendem Stress: „Dauert die mütterliche Belastung länger an, ist der CRH-Spiegel im Fruchtwasser erhöht", so Studienmitarbeiterin und Psychologin Pearl La Marca-Ghaemmaghami. Und diese höhere Konzentration des Stresshormons wiederum beschleunigte das Wachstum des Fetus. Damit wird der Effekt des Hormons auf das Wachstum bestätigt, wie er von Tieren bekannt ist. Das Corticotropin-Releasing-Hormon CRH spielt offenbar auch bei der Entwicklung des menschlichen Fetus eine komplexe und dynamische Rolle, die noch besser verstanden werden muss.
Schwangeren Frauen, die sich längeren Stresssituationen ausgesetzt sehen, raten die Psychologinnen, sich von einer psychologischen Fachperson unterstützen zu lassen, um die Belastungen besser zu bewältigen.