Ein seltener Keimzelltumor ist durch mehrere Strukturmerkmale gekennzeichnet, die eine endodermale extraembryonale Differenzierung (sekundärer Dottersack und Allantois) oder endodermale somatische Gewebe (Darm, Leber und Mesenchym) widerspiegeln. Diese Tumoren treten am häufigsten im zweiten oder dritten Lebensjahrzehnt auf. Sie sind typischerweise in den Keimdrüsen lokalisiert, gelegentlich auch in anderen Regionen.
Die Patienten stellen sich mit einer Gewebeverdichtung im Becken und/oder Unterleibsschmerzen (bei Frauen) oder einer oft schmerzlosen, einseitigen Hodenverdichtung (bei Männern) vor.
Die Rolle des Dottersacks in der embryonalen Entwicklung
Die Abfaltung des Embryos um seine Längsachse führt zur Einverleibung der dorsalen Anteile des Urdarms als primitiver Darm in den Embryo. Der Dottersack bleibt jedoch mit dem Darm über den Dottersackstiel in Verbindung. Die Dottersackwand besteht folglich aus Entoderm (Epithel) und Splanchnopleura (viszerales Mesoderm, Mesenchym).
Im Unterschied zum Vogel beinhaltet der Dottersack der Säugetiere keine Nährstoffe, sondern eine seröse Flüssigkeit. Bei Wiederkäuern und Schweinen, bei denen sich die Mesodermblätter bis zum abembryonalen Pol spalten, wird der Dottersack vollständig vom parietalen Mesoderm abgetrennt. Es kommt deshalb nicht zur Ausbildung einer Dottersackplazenta, und die vorübergehende Rolle des Dottersacks beschränkt sich auf die Blutbildung und die Ausbildung der Lebergefäße. Der Dottersack wird dementsprechend schnell zurückgebildet. Er bleibt lediglich als Anhängsel bestehen und wird Nabelbläschen genannt.
Bei Pferden und Fleischfressern hingegen, bei denen das Mesoderm am abembryonalen Pol ungespalten bleibt, wird das Chorion über die Dottersackgefäße vaskularisiert. Dabei entsteht eine funktionelle Dottersackplazenta, welche beim Pferd von der 10. bis zur 14. Woche bestehen bleibt und Ernährungsfunktionen übernimmt.
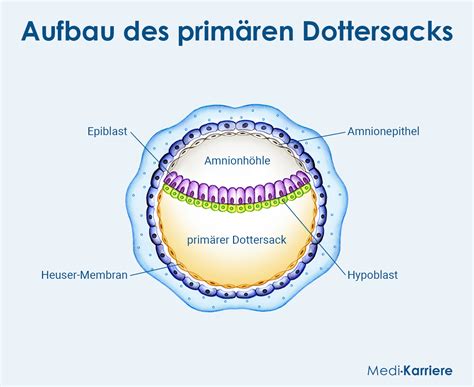
Gefäßsystem des Dottersacks und seine Verbindung zur Leber
Am abembryonalen Pol des Dottersacks bleiben Splanchnopleura und Somatopleura miteinander verbunden. Somit können über die Dottersackwand Gefäße an den Trophoblasten herangeführt werden. Die Blutgefäße, welche sich aus den Blutinseln der Dottersackwand entwickeln, koppeln an das embryonale Gefäßsystem und bilden einen geschlossenen Kreislauf.
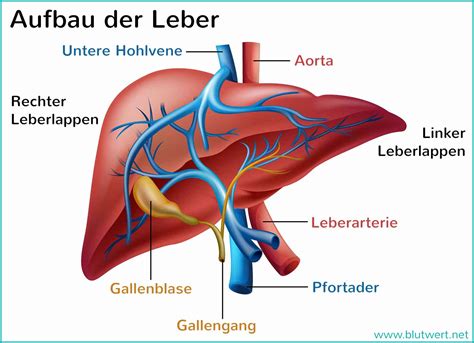
Vom Herz her kommend übernehmen die paarig angelegten Aa. vitellinae die arterielle Versorgung des Dottersacks und verzweigen sich in seinem Kapillargebiet. Die linke A. vitellina wird zurückgebildet, die rechte als A. mesenterica cranialis übernommen. Der venöse Abflussweg der Vena vitellina führt als Vena afferens hepatis zur Leber im Septum transversum und stellt als Vena efferens hepatis die Verbindung von der Leber zur V. cava caudalis und damit zum rechten Vorhof des Herzens her. Die V. afferens hepatis verbindet sich dabei mit der V. intestinalis (zukünftige V. portae).
Die rechte dorsale Aorta entlässt die bestehen bleibende A. vitellina, das Primordium der A. mesenterica cranialis. Vom venösen Rückfluss bleibt nur die rechte Hälfte bestehen. Die V. vitellina zieht als V. afferens zur Leber. Vorher verbindet sie sich mit der V. intestinalis zur V. portae, die sich in die Lebersinusoide verzweigt. Der proximale Abschnitt der V. vitellina verbindet die Leber mit der V. cava caudalis und wird als V. hepatica bezeichnet.
Keimblätter und ihre Bedeutung für die Organentwicklung
Die Bezeichnung „Keimblätter“ erleichtert das Verständnis der embryonalen Entwicklung, doch ist sie nicht immer intuitiv. Bei dreikeimblättrigen Tieren (allen bilateralsymmetrischen Tieren, also solchen mit einer linken und einer rechten Körperseite) und somit auch beim Menschen, entwickeln sich aus den Keimblättern verschiedene Gewebe und Organe.
- Aus der äußeren, oberen Schicht, dem Ektoderm, werden später unter anderem die Haut und das Nervensystem gebildet.
- Aus der inneren, nach konventioneller Darstellung untersten, zum Dottersack orientierten Schicht, dem Endoderm, gehen unter anderem der Verdauungstrakt, die Leber und die Lunge hervor.
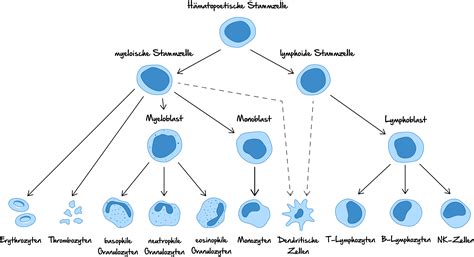
- Und die zuletzt durch Einwanderung von Zellen zwischen die beiden anderen Zelllagen entstandene mittlere Schicht, das Mesoderm, bringt später die Knochen, Muskeln und Nieren, das Herz und das Blut hervor - also auch die Stammzellen im Knochenmark, aus denen Immunzellen entstehen.
Immunzellen aus dem Dottersack: Eine neue Perspektive
Bis vor wenigen Jahren dachte man, all unsere Immunzellen seien Nachfahren der Stammzellen im Knochenmark. Dann entdeckte man, dass dies für Mikrogliazellen (makrophagenähnliche Zellen in unserem Gehirn) nicht zutrifft: Diese gehen vielmehr auf Vorläuferzellen zurück, die während der frühen Embryonalentwicklung noch vor der Schließung der Blut-Hirn-Schranke aus dem Dottersack ins spätere Gehirn einwandern. Diese Ur-Mikrogliazellen sind also extraembryonale Zellen, die zu keinem der drei Keimblätter gehören.
Inzwischen hat sich herausgestellt, dass dies auch auf viele andere Gewebsmakrophagen zutrifft. Zum Beispiel sind die Makrophagen, die im Herzmuskelgewebe Patrouille laufen und die Homöostase aufrechterhalten, teils direkt auf Vorläufer im Dottersack, teils auf Dottersackzellen-Nachfahren aus der fetalen Leber zurückzuführen. Diese Zellen sind offenbar ebenfalls imstande, sich ein Leben lang durch Teilung selbst zu erhalten.
Der Dottersack spielt auch eine Rolle bei der Entwicklung des Immunsystems Neugeborener. Lange glaubte man, Neugeborene seien so anfällig für Infektionen, weil ihr Immunsystem noch sehr unreif sei. Das Immunsystem wird aber in den ersten Lebenswochen aktiv unterdrückt, um eine Besiedlung des Darms mit lebensnotwendigen Bakterien und anderen Mikroorganismen zu ermöglichen. Dafür sind spezielle rote Blutkörperchen oder Erythrozyten zuständig, die den Oberflächenmarker CD71 tragen und vor allem in wenigen Wochen vor und nach der Geburt hergestellt werden. Sie produzieren das Enzym Arginase-2, das zu einem Mangel an der Aminosäure Arginin führt.
Makrophagen: Ordnungshüter der Organentwicklung
Die Entwicklungsbiologin Professorin Elvira Mass hat gezeigt, dass spezialisierte Immunzellen aus dem Dottersack des frühen Embryos, die sogenannten Makrophagen, eine tragende Rolle bei der Organentwicklung spielen. Wie Ordnungshüter treten sie in Aktion, wenn in den Organanlagen nicht alles nach Plan verläuft und tragen auch später zur Organgesundheit bei.
Bis dahin waren die Wissenschaftler fest davon überzeugt, dass die Gewebe-Makrophagen ausschließlich aus dem Knochenmark stammen. Mass hat gezeigt, dass auch der Dottersack ein wichtiger Ursprungsort ist und dass die Gewebe-Makrophagen aus dem Dottersack lebenslang zur Gesunderhaltung der Organe beitragen - oder ihnen schaden, wenn sie versagen.
Makrophagen gehören zum angeborenen Immunsystem der Säugetiere. Sie sind Teil eines permanent aktiven Überwachungssystems, das den Körper wie ein Radar ständig nach Bedrohungen durchforstet. Wenn das angeborene Immunsystem fündig wird, schlägt es Alarm und ruft das spezialisierte Immunsystem mit seinen maßgeschneiderten Antikörpern und Killerzellen auf den Plan. Makrophagen arbeiten als Putztruppe des angeborenen Immunsystems, die alles beseitigt, was nicht an Ort und Stelle gehört. Allerdings sind sie mehr als reine Fresszellen. Makrophagen produzieren auch Botenstoffe und schaffen Nährstoffe herbei. Damit sorgen sie dafür, dass nicht nur aufgeräumt wird, sondern auch Neues entsteht.
Jedes Organ hat sein eigenes Set an Gewebe-Makrophagen. Mass hat für Maus-Embryonen einen regelrechten Atlas mit den Wanderungsbewegungen der Vorläuferzellen aus dem Dottersack erstellt. Dabei wurde deutlich, dass diese Vorläuferzellen auf dem Weg zu den Organanlagen noch keine ausgereiften Gewebe-Makrophagen sind, sondern erst vor Ort ihre endgültige Bestimmung erlangen. In den Organanlagen bilden sie dann ein dreidimensionales Netzwerk, in das die organspezifischen Zellen nach und nach einsortiert werden, bis das Organ ausgereift ist.
Fehlfunktionen von Makrophagen und ihre Folgen
Wenn die Gewebe-Makrophagen so wichtig für die Entwicklung und Gesunderhaltung eines Organs sind, drängt sich die Frage auf, was passiert, wenn die Vorläuferzellen im Dottersack mutiert oder in besonderer Weise geprägt worden sind. Bei der Beantwortung dieser Frage kam Mass ein Befund aus der Medizin zur Hilfe. Es gibt Tumore, bei denen sich die Gewebe-Makrophagen unkontrolliert vermehren. Diese sogenannten Histiozytome weisen oft eine spezifische Mutation auf.
Mass hat diese Mutation bei Mäusen in die Vorläuferzellen des Dottersacks geschleust und verfolgt, wie sich die Tiere entwickelten. Konsequenzen zeigten sich vor allem bei den Mikroglia-Zellen. Sie wurden funktionell nachlässiger und begannen, benachbarte Neurone zu beseitigen. Früher oder später zeigten alle Tiere Schäden im Gehirn, die schließlich zu einer Lähmung führten.
„Diese Experimente beweisen, dass Makrophagen mit bestimmten Veränderungen zur Entstehung neurodegenerativer Erkrankungen beitragen“, sagt Mass über ihre Ergebnisse. „Obwohl es nur Tierexperimente sind, müssen wir uns jetzt natürlich fragen, was diese Befunde für die Entstehung neurodegenerativer Erkrankungen wie Alzheimer Demenz oder Morbus Parkinson bedeuten“, so die Nachwuchspreisträgerin weiter. „Vielleicht tragen nicht nur die bekannten Ablagerungen zur Entstehung beider Krankheiten bei, sondern auch das Fehlverhalten der Mikroglia, das durch eine Mutation in den Vorläuferzellen des Dottersacks entstanden ist oder durch eine spezielle, funktionell gleichartige unphysiologische epigenetische Prägung.“
Makrophagen und Knochenstoffwechsel
Mass hat sich auch für die Rolle der Makrophagen in anderen Geweben interessiert - etwa für die der Osteoklasten im Knochen. In einem gesunden Knochen halten sich Knochenaufbau und Knochenabbau die Waage. Für den Knochenaufbau sind die sogenannten Osteoblasten zuständig, für den Knochenabbau die Osteoklasten.
Mass konnte zeigen, dass ein Defekt im Wachstums- und Differenzierungsprogramm der Vorläuferzellen des Dottersacks dazu führt, dass keine funktionstüchtigen Osteoklasten entstehen. Dadurch gerät die Balance zwischen Knochenaufbau und Knochenabbau durcheinander. Mäuse mit einem entsprechenden Defekt behelfen sich, indem sie nach der Geburt Unterstützung aus dem Knochenmark holen und von dort neue Makrophagen rekrutieren. Patienten mit einer Knochenverhärtung, einer sogenannten Osteopetrose, können das nicht, denn anders als bei den Mäusen, bei denen Mass den Defekt nur in die Vorläuferzellen des Dottersacks geschleust hat, ist bei den Patienten jede Zelle mutiert, auch die Zellen des Knochenmarks. Sie können daher keine Hilfe von dort erwarten. Allerdings könnte ihnen möglicherweise eine Bluttransfusion von gesunden Spendern helfen.
Zukünftige Forschungsperspektiven
Mass wird in Zukunft auch untersuchen, welche Umweltfaktoren die epigenetische Prägung in den Vorläuferzellen des Dottersacks verändern und wie diese Veränderungen die Funktion der späteren Gewebe-Makrophagen beeinflussen. „Ich bin der festen Überzeugung, dass viele Erkrankungen ihre Ursache in solchen Prägungen und Veränderungen haben“, sagt Mass über ihr Forschungsvorhaben.
Sie will zum Beispiel den Einfluss mütterlicher Fettleibigkeit bei Mäusen untersuchen. Mass hegt die Vermutung, dass die Nachkommenschaft übergewichtiger Mäuse eine Fettleber entwickeln, weil die Kupffer-Zellen (spezifische Leber-Makrophagen) in Mitleidenschaft gezogen worden sind. Mit finanzieller Förderung der Europäischen Union wird sie in den kommenden Jahren auch den Einfluss von Nanoplastik-Partikeln aus der Umwelt auf Makrophagen untersuchen.
Der Dottersackkreislauf
Der Dottersackkreislauf ist der Blutkreislauf des Embryos bei Wirbeltieren zum Stofftransport in der Dottersack-Plazenta. Er entsteht beim menschlichen Embryo in der dritten Schwangerschaftswoche aus Blutinseln im Dottersack, welche von Angioblasten umgeben werden. Diese differenzieren sich zur Gefäßwand der Arteriae und Venae omphalomesentericae. Der Dotterkreislauf liegt außerhalb des Embryos und steht über die Gefäße im Dottersackstiel mit dem Blutkreislauf des Embryos bzw. Fötus in Verbindung.
Bei den Säugetieren bildet sich der Dottersackkreislauf noch während der Fötalentwicklung zurück, bei Pferden ist er relativ lange aktiv. Da der Dottersack bei höheren Säugetieren keine Nährstoffe enthält, ist der Dottersackkreislauf für die Embryonalentwicklung ohne Bedeutung; an seine Stelle tritt der Plazentarkreislauf.
Bei Vögeln entsteht der Dottersackkreislauf ebenfalls in der Wand des Dottersacks und wird von der Arteria vitellina dextra und sinistra sowie der Vena vitellina anterior und posterior gebildet. Die beiden Venen anastomieren miteinander und bilden einen kranzförmigen Blutleiter, den Sinus terminalis. Von den Venae vitellinae fließt das Blut zum Sinus venosus des Herzens und über die Arteriae vitellinae wieder in den Dottersack zurück. Beim Haushuhn ist der Dottersackkreislauf bereits am zweiten Bebrütungstag funktionsfähig.
Schwangerschaft - So entsteht ein kleines Wunder (Animation)
tags: #dottersack #und #leber