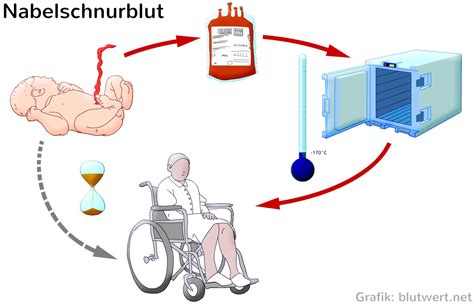
Nach der Geburt eines Neugeborenen verbleibt in der Nabelschnur und im kindlichen Anteil des Mutterkuchens (Plazenta) eine erhebliche Menge an Stammzellen. Dieses Stammzellmaterial, das normalerweise verworfen wird, kann für eine allogene Stammzelltransplantation bei einem Kind mit entsprechenden Erkrankungen von unschätzbarem Wert sein. Wenn die Eltern zustimmen, kann dieses wertvolle Gewebe anonym an eine öffentliche, zentrale Nabelschnurblutbank gespendet werden.
Obwohl das gewonnene Material aufgrund der Unreife der Zellen sowohl Vor- als auch Nachteile mit sich bringt, stellt es eine zusätzliche und wichtige Option für Kinder dar, die anderweitig keinen passenden Spender finden. Es ist zu betonen, dass Stammzellen aus Nabelschnurblut derzeit nur allogen transplantiert werden. Die Wahrscheinlichkeit, dass ein Kind zu einem späteren Zeitpunkt eigene Stammzellen benötigt, ist sehr gering. Bei gutartigen Bluterkrankungen im Kindes- und Jugendalter sowie bei angeborenen Immundefekten und Stoffwechselerkrankungen ist eine autologe Transplantation mit eigenem, eingefrorenem Nabelschnurblut nicht möglich.
Eindeutige Statistiken über den individuellen zukünftigen Bedarf an eigenen Nabelschnurblut-Stammzellen existieren nicht. Schätzungen aus den USA bewegen sich beispielsweise zwischen 1:1.000 und 1:200.000. Die Gewinnung von Nabelschnurblut-Stammzellen ist ein einfacher, sicherer und schmerzfreier Prozess, der keinerlei Risiko für Mutter und Kind birgt. Zwischen 60 und 200 Milliliter des wertvollen Nabelschnurbluts können durch Punktion der Nabelschnurvene gewonnen werden.
Rhesus-Inkompatibilität: Ursachen und Folgen
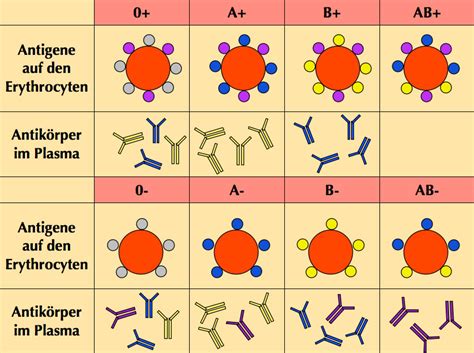
Die Rhesusfaktoren sind Eiweißstrukturen auf der Oberfläche der roten Blutkörperchen. Das wichtigste Merkmal ist der Rhesusfaktor D. Etwa 85 % der Bevölkerung in Europa sind Rhesus-positiv (Rh+) und tragen dieses Antigen auf ihren Erythrozyten, während Rhesus-negative (Rh-) Menschen es nicht besitzen. Eine Rhesus-Sensibilisierung kann entstehen, wenn Rhesus-positives Blut in den Körper eines Rhesus-negativen Menschen gelangt, sei es durch Bluttransfusionen oder unter bestimmten Umständen während der Schwangerschaft und Geburt.
Die Blutkreisläufe von Mutter und ungeborenem Kind sind normalerweise durch die Plazenta getrennt. Dennoch können geringe Mengen kindlicher Erythrozyten in den mütterlichen Kreislauf gelangen. Dies kann bei invasiven Eingriffen während der Schwangerschaft, bei Verletzungen, Blutungen oder während der Geburt geschehen. Wenn eine Rhesus-negative Mutter mit einem Rhesus-positiven Kind schwanger ist, kann ihr Immunsystem durch den Kontakt mit dem kindlichen D-Antigen sensibilisiert werden und Antikörper gegen dieses Antigen bilden.
Im Gegensatz zu den Erythrozyten können diese D-Antikörper (Immunglobuline vom Typ G) die Plazentaschranke überwinden und in den Blutkreislauf des Kindes gelangen. Dort binden sie an die RhD-positiven Erythrozyten des Kindes, was zu deren vorzeitigem Abbau in der Milz führt. Dieser Prozess, bekannt als Hämolyse der Erythrozyten, kann beim Kind zu Anämie und Hyperbilirubinämie führen.
Der Verlauf einer Rhesus-Inkompatibilität
Bei der ersten Schwangerschaft einer Rhesus-negativen Frau mit einem Rhesus-positiven Kind verläuft die Sensibilisierung in der Regel langsam und führt meist nicht zu Problemen für das erste Kind. Wenn die Mutter jedoch erneut mit einem Rhesus-positiven Kind schwanger ist, kann ihr Immunsystem aufgrund von Gedächtniszellen eine schnellere und stärkere Antikörperbildung (Boosterung) auslösen.
Die Folgen für das Kind können vielfältig sein:
- Milde Hämolyse mit leichtem Neugeborenenikterus (Gelbsucht).
- Deutlichere Anämie mit vergrößerter Leber und Milz (Hepatosplenomegalie) aufgrund gesteigerter Blutbildung außerhalb des Knochenmarks.
- Schwerer Ikterus (Neugeborenenikterus), oft schon bei Geburt vorhanden (Ikterus gravis et praecox).
- Bei starker Hämolyse kann Biliverdin und Bilirubin freigesetzt werden, das sich auch im Dentin des Zahnes ablagert und zu blaugrüner Verfärbung der Zahnkronen und -wurzeln führt (Erythroblastose).
- Im schlimmsten Fall kann es zu Hydrops fetalis (Wassersucht des Fötus) kommen, was zu Missbildungen oder sogar zum Tod des Ungeborenen oder Neugeborenen führen kann. Dieses vorgeburtliche Bild wird nach der Geburt als Morbus haemolyticus neonatorum (MHN) bezeichnet.
Der Schweregrad eines Morbus haemolyticus neonatorum hängt von der Konzentration der mütterlichen Antikörper, dem Anteil der plazentagängigen IgG-Antikörper und der Antigendichte auf den kindlichen Erythrozyten ab, was wiederum den Grad der Hämolyse bestimmt.
Diagnostik und Prävention der Rhesus-Inkompatibilität
Für die Diagnostik der Rhesus-Inkompatibilität sind mehrere Schritte entscheidend:
- Blutgruppenbestimmung von Mutter und Kind zu Beginn der Schwangerschaft.
- Indirekter Coombs-Test: Zum Nachweis plazentagängiger IgG-Antikörper im mütterlichen Serum.
- Direkter Coombs-Test: Zum Nachweis von Antikörpern auf den Erythrozyten des Kindes.
- Polymerase-Kettenreaktion (PCR): Ermöglicht die zuverlässige Bestimmung des RhD-Status des Fetus aus dem Blut der Mutter ab der 34. bis 36. Schwangerschaftswoche.
Um die Folgen einer Rhesus-Inkompatibilität zu verhindern oder zu minimieren, wird die Anti-D-Prophylaxe eingesetzt. Dieses Medikament enthält Anti-D- bzw. Rhesusfaktor-Antikörper (humanes Anti-D-Immunglobulin) und wird als Passiv-Immunisierung der Frau verabreicht.
Die Anti-D-Prophylaxe
Die Anti-D-Prophylaxe wird Rhesus-negativen Schwangeren in der Regel in der 28. bis 30. Schwangerschaftswoche und erneut innerhalb von 72 Stunden nach der Geburt eines Rhesus-positiven Kindes verabreicht. Die Injektion von Anti-D-Immunglobulin verhindert, dass das mütterliche Immunsystem Antikörper gegen die kindlichen Erythrozyten bildet, indem die injizierten Antikörper die kindlichen roten Blutkörperchen abfangen, bevor das mütterliche Immunsystem reagieren kann.
Auch nach invasiven Eingriffen in der Gebärmutter (z.B. Chorionzottenbiopsie, Amniozentese, Nabelschnurpunktion), nach Verletzungen, Blutungen, Fehlgeburten oder nach der Verabreichung von Rhesus-unverträglichen Bluttransfusionen wird eine Anti-D-Prophylaxe empfohlen.
Seit dem 1. Juli 2021 ist in Deutschland ein pränataler Bluttest zur Bestimmung des Rhesusfaktors des Kindes aus dem Blut der Mutter eine Leistung der gesetzlichen Krankenkassen. Dieser Test kann ab der zwölften Schwangerschaftswoche durchgeführt werden und ermöglicht eine gezielte Rhesusprophylaxe, wodurch unnötige Spritzen bei Rhesus-negativen Babys vermieden werden können. Bei Mehrlingsschwangerschaften oder wenn die Frau sich gegen den Test entscheidet, wird weiterhin die routinemäßige Prophylaxe durchgeführt.
Rhesusunverträglichkeit + Rhesusprophylaxe - Rhesusfaktor einfach erklärt! (+ Infos zum neuen Test!)
Historischer Kontext und Entwicklung der Prophylaxe
Der Impfstoff zur Anti-D-Prophylaxe wurde in den 1960er Jahren von britischen und US-amerikanischen Forschergruppen entwickelt und 1969 eingeführt. Zuvor gab es Fälle von Hepatitis C-Infektionen bei RhD-negativen Müttern in der DDR, die im Rahmen der damals vorgeschriebenen Anti-D-Prophylaxe kontaminiertes Serum erhielten. Diese Vorfälle wurden der Öffentlichkeit lange Zeit vorenthalten.
Bis etwa 2020 wurden in Deutschland Anti-D-Immunglobuline bei allen RhD-negativen Schwangeren prophylaktisch angewendet. Mit der Einführung des pränatalen Tests konnte die Anzahl der unnötigen Behandlungen reduziert werden, obwohl die Wirksamkeit der Prophylaxe bei tatsächlicher Inkompatibilität (>99 %) außer Frage steht.
Nabelschnurblutspende: Eine wertvolle Ressource
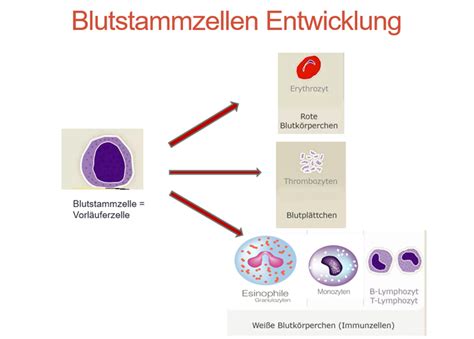
Das Nabelschnurblut, das nach der Geburt in der Nabelschnur und Plazenta verbleibt, ist eine reiche Quelle für Blutstammzellen. Diese Stammzellen sind die Bausteine des Lebens und können sich zu über 200 verschiedenen Zellarten entwickeln. Ihre natürlichen Aufgaben umfassen Aufbau, Regeneration und Reparatur des Körpers.
Die Spende von Nabelschnurblut ist ein einfacher, sicherer und schmerzfreier Prozess für Mutter und Kind. Das gewonnene Blut wird aufbereitet und in einer Nabelschnurblutbank eingelagert. Diese Stammzellen können Leben retten, indem sie bei Patienten mit gestörten blutbildenden Systemen, insbesondere bei verschiedenen Formen von Leukämie und Immundefekten, eine Heilung ermöglichen.
Im Gegensatz zu anderen Methoden der Stammzellspende ist die Nabelschnurblutspende schnell verfügbar und erfordert keine aufwändige Vorbereitung des Spenders. Zudem ist eine Transplantation von Nabelschnurblutstammzellen auch bei geringerer Übereinstimmung der Gewebemerkmale (HLA-Merkmale) möglich.
Nabelschnurblutspende und Rhesusfaktor
Die Frage des Rhesusfaktors spielt bei der Nabelschnurblutspende eine untergeordnete Rolle. Es ist jedoch wichtig zu wissen, dass die Rhesus-Inkompatibilität die Gesundheit des Kindes beeinträchtigen kann, während die Spende von Nabelschnurblut eine potenziell lebensrettende Maßnahme für andere darstellt.
Es gab Diskussionen darüber, ob das "Auspulsieren" der Nabelschnur bei Rhesus-negativen Müttern unbedingt erfolgen sollte. Während das Auspulsierenlassen der Nabelschnur als vorteilhaft für das Neugeborene gilt, um einen sanften Start ins Leben zu ermöglichen, war die Sorge, dass bei Rhesus-negativen Müttern ein früherer Abnabelungsschritt notwendig sein könnte, um den Blutkontakt zu minimieren. Moderne medizinische Verfahren und die Anti-D-Prophylaxe haben jedoch dazu beigetragen, diese Bedenken weitgehend auszuräumen.
Die Entscheidung zur Nabelschnurblutspende sollte unabhängig vom Rhesusfaktor der Mutter getroffen werden, solange keine medizinischen Kontraindikationen vorliegen. Die Gewinnung von Nabelschnurblut hat stets oberste Priorität für die Gesundheit von Mutter und Kind.
Zusammenfassung und wichtige Hinweise
Die Rhesus-Inkompatibilität stellt eine potenzielle Gefahr für das ungeborene Kind dar, kann aber durch frühzeitige Diagnostik und die konsequente Anwendung der Anti-D-Prophylaxe heute effektiv verhindert werden. Die Einführung des pränatalen Bluttests hat die Prophylaxe weiter optimiert.
Die Spende von Nabelschnurblut ist eine altruistische Handlung, die das Leben von Patienten mit schweren Erkrankungen retten kann. Sie ist sicher, schmerzfrei und stellt eine wertvolle Ressource im medizinischen Fortschritt dar. Nicht jedes gespendete Nabelschnurblut ist für die klinische Anwendung geeignet, doch auch für die Forschung kann es von großem Wert sein.
Es ist ratsam, sich frühzeitig mit dem behandelnden Arzt oder der Klinik über die Möglichkeiten der Nabelschnurblutspende und die Handhabung des Rhesusfaktors während der Schwangerschaft zu informieren.
tags: #nabelschnurblut #spenden #rhesus #negativ #spritze