Die moderne Medizin stützt sich maßgeblich auf diagnostische Bildgebung und Strahlentherapie, die den Patienten zweifellos zugutekommen. Es ist jedoch unerlässlich, die mit der Anwendung ionisierender Strahlung verbundenen Risiken zu berücksichtigen.
Grundlagen ionisierender Strahlung
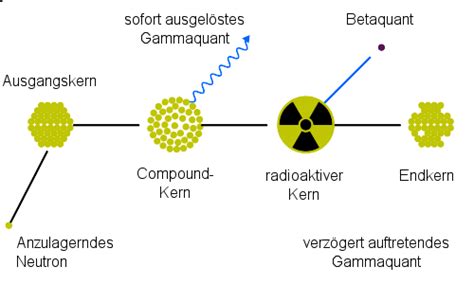
Ionisierende Strahlung tritt in Form von Alpha-, Beta- oder Gammastrahlung auf, die aus radioaktiven Zerfallsprozessen resultiert. Alpha- und Beta-Strahlung sind Teilchenstrahlung, während Gammastrahlung eine Form der elektromagnetischen Strahlung darstellt. Radioaktive Elemente sind natürlicherweise in unserer Umwelt vorhanden und tragen zur jährlichen natürlichen Strahlenexposition bei, deren Höhe von Faktoren wie Bodenbeschaffenheit und Meereshöhe abhängt.
Elektromagnetische Strahlung kann auch künstlich erzeugt werden, beispielsweise in einer Röntgenröhre oder einem Linearbeschleuniger. Dort werden Elektronen auf ein Target geschossen, was durch verschiedene Wechselwirkungen mit den Atomen elektromagnetische Strahlung erzeugt. Je nach Energiebereich spricht man von Röntgenstrahlung (0,1-250 keV) oder Gammastrahlung (ab 250 keV). Diese Strahlung durchdringt den menschlichen Körper mit einer graduierten, gewebeabhängigen Abschwächung, wobei Energie an das Gewebe übertragen wird. Diese Energieübertragung wird als Strahlendosis ausgedrückt.
Wirkung ionisierender Strahlung auf Zellen
Die Energieübertragung ionisierender Strahlung an Materie kann zur Ionisation von Molekülen führen, im Körper primär von Wassermolekülen. Über nachfolgende chemische Reaktionen können lebenswichtige Zellstrukturen wie die DNA beschädigt werden. Zellen verfügen über effiziente Reparaturmechanismen, die in den meisten Fällen eine erfolgreiche Reparatur und Weiterexistenz der Zelle ermöglichen.
Manchmal können jedoch durch fehlerhafte Regeneration mutierte Zellen entstehen, die lebens- und fortpflanzungsfähig sind. Über einen langen Zeitraum können diese zu einer mutierten Zellpopulation heranwachsen, was als stochastischer Effekt bezeichnet wird. Dazu zählen Krebserkrankungen oder genetische Veränderungen in den Keimzellen, die sich als Erkrankungen der Folgegeneration manifestieren können.
Eine einzelne mutierte Zelle kann einen stochastischen Effekt auslösen; mehrere Mutationen verstärken den Effekt nicht, erhöhen aber die Wahrscheinlichkeit seines Auftretens. Nach dem aktuellen «Linear No-Threshold»-Modell können bereits kleinste Strahlendosen solche Effekte bewirken, wobei die Wahrscheinlichkeit linear mit der Dosis steigt. Die unterschiedliche Anfälligkeit von Organen für Mutationen wird durch Gewebewichtungsfaktoren (wT) beschrieben, die auf statistischen Untersuchungen basieren.
Die effektive Dosis (E) in Sievert [Sv] gibt eine Risikoabschätzung für eine einzelne Exposition an, indem Organdosen mit den jeweiligen Gewichtungsfaktoren multipliziert und aufsummiert werden. Ein zusätzliches Krebsrisiko von 5% pro Sievert wird angenommen.
Deterministische und stochastische Effekte
In Fällen, in denen zelluläre Reparaturmechanismen versagen, stirbt die Zelle ab. Dies wird als deterministischer Effekt bezeichnet. Die Anzahl abgestorbener Zellen ist proportional zur applizierten Dosis. Organe können kleinere Zellverluste kompensieren, jedoch treten ab einer organspezifischen Schwellendosis Schäden auf, die mit zunehmender Dosis stärker werden und bis zum Funktionsverlust führen können.
Typische Schwellendosen reichen von 100 mGy für Veränderungen im Blutbild bis zu etwa 5 Gy für Hautläsionen. Deterministische Effekte werden gezielt in der Strahlentherapie zur Zerstörung von Tumorgewebe eingesetzt, wobei die Minimierung von Schäden im umliegenden gesunden Gewebe entscheidend ist. Typische Bestrahlungsdosen liegen bei etwa 50 Gy, aufgeteilt in Einzelsitzungen von 2 Gy.
Strahlenempfindlichkeit bei Frauen und im gynäkologischen Kontext
Im gynäkologischen Bereich liegt ein besonderes Augenmerk auf den Reproduktionsorganen und dem ungeborenen Kind. Ovarien- und Uterusdosen im Bereich von 2-3 Gy können bei Mädchen und Frauen zu Unfruchtbarkeit führen, was insbesondere bei Strahlentherapie im Abdomenbereich berücksichtigt werden muss. Im diagnostischen Kontext sind solche Dosen unwahrscheinlich.
Früher wurde von einer erhöhten Wahrscheinlichkeit für vererbbare genetische Veränderungen als stochastischer Effekt ausgegangen. Diese konnten jedoch nie beobachtet werden, sodass heute von einem sehr geringen genetischen Risiko durch Exposition der Eizellen ausgegangen wird, das im diagnostischen Dosisbereich meist vernachlässigbar ist.
Strahlenexposition während der Schwangerschaft
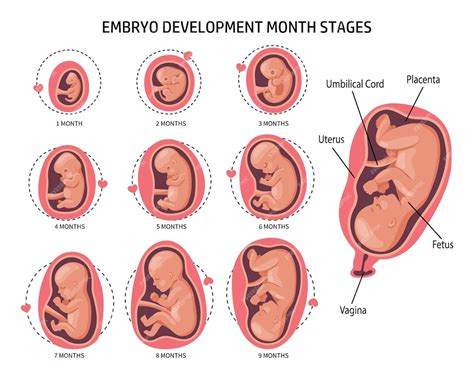
Das Risiko für das ungeborene Kind während der Schwangerschaft ist stark vom Zeitpunkt der Exposition abhängig. Deterministische Effekte betreffen besonders die sich entwickelnden Organe oder Organsysteme.
- Präimplantationsphase: Eine Strahlenexposition von mehr als 100 mGy kann zum Fruchttod führen; darunter sind keine Auswirkungen zu erwarten.
- Organogenese (ca. 4. bis 10. Schwangerschaftswoche): Strahlendosen ab 100 mGy können Fehlbildungen verursachen; bei sehr hohen Dosen ist Fruchttod möglich.
- Fötalphase (ab ca. 10. Schwangerschaftswoche): Ab Schwellenwerten von 100-500 mGy können Wachstumsverzögerungen und Beeinträchtigungen der intellektuellen Entwicklung auftreten.
Bei der diagnostischen Bildgebung bleiben die Dosen für das ungeborene Kind typischerweise weit unter diesen Schwellenwerten. Dennoch ist jede Strahlenexposition mit einem leicht erhöhten stochastischen Risiko verbunden.
Im klinischen Setting sollte nach einer Exposition die Dosis von Fachpersonen abgeschätzt werden. Die Praxis, die die Exposition durchgeführt hat, ist die erste Anlaufstelle und leitet bei Bedarf weitere Schritte ein, beispielsweise durch Medizinphysiker.
Individuelle Strahlenempfindlichkeit und genetische Faktoren
Die individuelle Strahlenempfindlichkeit beschreibt die Fähigkeit von Zellen, durch Strahlung verursachte DNA-Schäden zu reparieren und die Information über Schäden korrekt weiterzugeben. Dies beinhaltet die Aktivierung von Tumorsuppressorproteinen zur Zellteilungshemmung und die Auslösung von vorzeitiger Seneszenz oder Zelltod bei schweren Schäden.
Veränderungen in den Genen, die für die Schadensprozessierung zuständig sind, können zu einer erhöhten Strahlenempfindlichkeit führen. Genetische Erkrankungen wie das Fanconi-Syndrom, Ataxia Telangiectatica und das Nijmegen Breakage Syndrom sind mit einer erhöhten Strahlenempfindlichkeit assoziiert.
Genetische Syndrome mit erhöhter Strahlenempfindlichkeit umfassen:
- Ataxia Telangiectatica (ATM)
- ATLD / Mre11
- Cockayne-Syndrom
- Bloom-Syndrom
- DNA-PK
- Fanconi Anämie
- Ligase IV
- Nijmegen Breakage Syndrom
- Rett Syndrom
- Rothmund-Thomson-Syndrom
- SCID-Artemis
- Trichothiodystrophie
- Werner-Syndrom
- Xeroderma pigmentosum
Zudem können familiär weitergegebene Gene, die keine Erkrankung verursachen, aber zu familiär gehäuften Krebserkrankungen führen, ebenfalls mit einer erhöhten Strahlenempfindlichkeit in Zusammenhang stehen. Ein Hinweis darauf können multiple Krebserkrankungen bei Geschwistern oder Eltern in jüngerem Alter sein.
Besonderheiten bei Kindern und Jugendlichen
Kinder teilen sich ihre Zellen schneller als Erwachsene, was ihre Empfindlichkeit gegenüber ionisierender Strahlung erhöht. Die Indikation zur Anwendung ionisierender Strahlung bei Kindern wird daher besonders sorgfältig geprüft. Das Bundesamt für Strahlenschutz (BfS) betont den besonderen Schutzbedarf von Kindern bei Strahlenanwendungen in der Medizin, da sie ein deutlich höheres Risiko haben, an Leukämie zu erkranken.
Die noch nicht vollständig entwickelte Reparaturfähigkeit von DNA-Schäden trägt zur höheren Strahlenempfindlichkeit von Kindern bei. Studien zeigen, dass bei Kindern nach Bestrahlung häufiger Chromosomenschäden nachgewiesen werden als bei Erwachsenen.
Die Berechnung einer effektiven Dosis berücksichtigt stets die Empfindlichkeit des Gewebes, wie in der Publikation Nr. 103 der ICRP festgelegt. Die empfindlichsten Gewebe sind das rote Knochenmark, Mundschleimhaut, Magen, Gallenblase, Bauchspeicheldrüse, Dünn- und Dickdarm, Brust, Thymusdrüse, Atemwege inkl. Lunge, Herz, Nieren, Nebennieren, Milz, Lymphknoten, Muskelgewebe sowie die Prostata und Keimdrüsen.
Risikobewertung und Schutzmaßnahmen
Um das Risiko strahleninduzierter Erkrankungen abzuschätzen, sind Tests geplant, die Ärzten Entscheidungshilfen für die Wahl der Therapie-Methode, insbesondere bei Krebspatienten, liefern sollen. Die Ärzteorganisation IPPNW fordert eine verstärkte Berücksichtigung des Strahlenschutzes für Kinder.
Die Strahlenexposition eines Embryos und Fetus sollte nach Möglichkeit vermieden werden. Schwangere Frauen, die zu Untersuchungen erscheinen, müssen befragt werden, ob sie schwanger sind. Wenn eine Schwangerschaft nicht ausgeschlossen werden kann, ist die Notwendigkeit der Strahlenanwendung unter sorgfältiger Nutzen-Risiko-Abwägung zu prüfen.
Bei Untersuchungen mit hoher Uterus-Exposition gibt es zwei Möglichkeiten: Bei Verdacht auf eine Schwangerschaft im ersten Zyklusdrittel kann die Untersuchung auf die ersten 10 Tage des nächsten Zyklus verschoben werden, wenn die Situation dies zulässt. Eine unbeabsichtigte Strahlenexposition eines Embryos oder Feten bei üblichen radiologischen Verfahren birgt ein so geringes Risiko, dass invasive diagnostische Prozeduren oder ein Schwangerschaftsabbruch meist nicht gerechtfertigt sind. Der anwendende Arzt sollte jedoch eine individuelle Bewertung auf Basis der Expositionsdaten vornehmen und mit der werdenden Mutter besprechen.
Auch bei der Magnetresonanztomografie (MRT) und Kontrastmittelapplikationen ist während der Schwangerschaft Vorsicht geboten. Die Indikation zu MRT-Untersuchungen im ersten Trimenon ist besonders streng zu stellen.
Fukushima: Erhöhte Strahlenbelastung in der Schwangerschaft
Aktuelle Forschung und Studienergebnisse
Eine aktuelle Studie, veröffentlicht in Radiation Research, untersuchte die individuelle Strahlenempfindlichkeit und die Rolle genetischer Faktoren. Die Ergebnisse deuteten darauf hin, dass die Bedeutung der Strahlenexposition als Hauptfaktor für die Strahlenempfindlichkeit unterstrichen wird, während eine relevante genetische Komponente in dieser spezifischen Untersuchung nicht nachgewiesen werden konnte. Die personalisierte Deeskalation der Radiotherapie bei Patienten mit angeborener erhöhter Strahlensensitivität ist in der täglichen Routine offenbar nicht anwendbar.
Zusammenfassung der Effekte
- Deterministische Wirkungen entstehen durch massive Zellabtötung und führen zu Organschäden oberhalb einer Schwellendosis.
- Stochastische Wirkungen resultieren aus DNA-Veränderungen und erhöhen die Wahrscheinlichkeit für Krebserkrankungen, wobei die Latenzzeit variieren kann.
Fehlbildungen und Entwicklungsstörungen beim ungeborenen Kind zählen zu den deterministischen Wirkungen. Die Dosis-Schwellenwerte für diese Effekte liegen im Bereich von 50 bis 100 Millisievert (mSv) für die Gebärmutter.
Die Wahrscheinlichkeit für stochastische Spätschäden ist unabhängig von der Entwicklungsphase des Ungeborenen. Das Krebsrisiko, insbesondere das Leukämierisiko, ist nach einer Strahlenbelastung im Mutterleib erhöht.
tags: #wann #sind #embryos #am #strahlenempfindlichsten