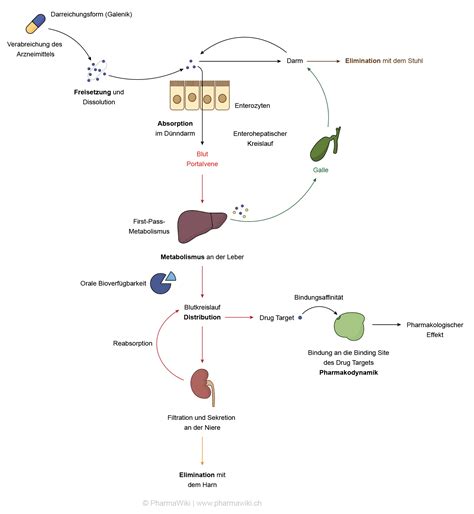
Der Wirkstoff Theophyllin, chemisch bekannt als 1,3-Dimethylxanthin, findet Anwendung bei der Behandlung verschiedener Atemwegserkrankungen wie der chronisch obstruktiven Lungenerkrankung (COPD) und Asthma. Die genauen Wirkungsmechanismen von Theophyllin sind bis heute nicht vollständig geklärt. Eine Rolle spielt offenbar die Hemmung der Phosphodiesterase, was zu einem Anstieg des intrazellulären cAMP führt, jedoch scheint dies nur bei Konzentrationen im oberen therapeutisch genutzten Bereich relevant zu sein.
Nach oraler Gabe wird Theophyllin vollständig resorbiert. Der Wirkstoff zeichnet sich durch eine geringe therapeutische Breite aus, wobei die wirksame Serumkonzentration zwischen 5 und 12 µg/ml liegt. Eine Überschreitung von 20 µg/ml sollte unbedingt vermieden werden. Sobald der Mindestserumspiegel von etwa 5 μg/ml erreicht ist, tritt die bronchodilatatorische Wirkung innerhalb von Minuten ein.
Die Plasmaproteinbindung von Theophyllin beträgt beim Erwachsenen etwa 60%, während sie bei Neugeborenen und Erwachsenen mit Leberzirrhose auf ca. 40% sinkt. Der Metabolismus von Theophyllin erfolgt hauptsächlich über das Enzym CYP1A2, und die Ausscheidung erfolgt über die Nieren. Beim Erwachsenen werden etwa 7 bis 13% der Substanz unverändert im Harn ausgeschieden. Bei Neugeborenen sind die Verhältnisse anders, wobei 3-Methyl-Xanthin einer der Hauptmetaboliten ist.
Interindividuelle Unterschiede in der hepatischen Metabolisierung, bedingt durch Faktoren wie Alter, Körpergewicht, Ernährung, Rauchen (Induktion von CYP1A2), Begleitmedikation sowie Erkrankungen von Herz, Lunge, Leber und Virusinfektionen, können die Clearance, die Serumkonzentrationen und die Eliminationshalbwertszeiten erheblich beeinflussen. Dies unterstreicht die Notwendigkeit einer individuellen Dosierung von Theophyllin, die sich nach der Wirkung und den Theophyllin-Serumkonzentrationen richten sollte. Ein anzustrebender Bereich liegt hierbei zwischen 8 und 20 μg/ml.
Bei unzureichender Wirksamkeit oder dem Auftreten unerwünschter Wirkungen sind Kontrollen des Theophyllin-Serumspiegels unerlässlich. Da Theophyllin nicht vom Fettgewebe aufgenommen wird, ist für die Dosisermittlung das Normalgewicht als Referenz heranzuziehen.
Für erwachsene Raucher gilt eine Besonderheit: Sie benötigen im Vergleich zu nichtrauchenden Erwachsenen eine höhere körpergewichtsbezogene Theophyllin-Dosis, da die Eliminationsrate erhöht ist.
Die gleichzeitige Anwendung von Arzneimitteln, die das Enzym CYP1A2 beeinflussen, kann zu Änderungen im Theophyllin-Abbau führen. Dazu gehören beispielsweise Barbiturate und bestimmte Calciumkanalantagonisten.
Theophyllin in Schwangerschaft und Stillzeit
Zur Anwendung von Theophyllin während des ersten Schwangerschaftstrimenons liegen keine ausreichenden Erfahrungen vor, weshalb eine Anwendung in dieser Zeit vermieden werden sollte. Im zweiten und dritten Trimenon sollte Theophyllin nur nach strenger Nutzen-Risiko-Abwägung eingesetzt werden, da es die Plazenta passiert und im Fötus sympathomimetisch wirken kann.
Mit fortschreitender Schwangerschaft können die Plasmaproteinbindung und die Clearance von Theophyllin abnehmen, was eine Dosisreduktion zur Vermeidung unerwünschter Wirkungen erforderlich machen kann. Eine Behandlung mit Theophyllin am Ende der Schwangerschaft kann zudem zu einer Wehenhemmung führen.
Theophyllin geht in die Muttermilch über, und es können therapeutische Serumkonzentrationen beim gestillten Kind erreicht werden. Daher sollte die Dosis bei stillenden Patientinnen so niedrig wie möglich gehalten werden, und das gestillte Kind muss sorgfältig auf mögliche Theophyllin-Wirkungen hin überwacht werden.
Es gibt Studien mit über 500 ausgewerteten Schwangerschaften, die keinen Hinweis auf ein relevant erhöhtes Fehlbildungsrisiko erbracht haben, wenngleich einige Studien methodische Schwächen aufweisen. In verschiedenen Studien zeigte sich keine Assoziation mit Totgeburten oder geringem Geburtsgewicht. Ein erhöhtes Risiko für Präeklampsie und Frühgeburtlichkeit wurde diskutiert, wobei der Einfluss anderer mütterlicher Faktoren unklar bleibt.
In der Stillzeit sind pharmakokinetische Untersuchungen durchgeführt worden, die darauf hindeuten, dass ein gestilltes Kind durch eine Mahlzeit maximal eine bestimmte Menge Theophyllin aufnimmt. Dennoch kann es je nach mütterlichem Plasmaspiegel und kindlicher Clearance-Rate zu einer Akkumulation beim gestillten Säugling kommen. Theophyllin kann in der Stillzeit verwendet werden, wobei die Dosis so niedrig wie therapeutisch möglich gewählt und das gestillte Kind sorgfältig überwacht werden sollte.
Besonderheiten bei Früh- und Neugeborenen
Medikamentöse Vorsorge und häufige Behandlungssituationen bei Früh- und Neugeborenen stellen eine besondere Herausforderung dar. Für viele Wirkstoffe fehlen belastbare Studiendaten zur Anwendung bei dieser Patientengruppe. Die Wirksamkeit und Sicherheit wurden nicht systematisch untersucht, und die Dosierung erfolgte oft empirisch oder basierend auf Erfahrungswerten. Ein europäischer Review von 2018 zeigte, dass bis zu 99,5 Prozent der Patienten auf Neugeborenen-Intensivstationen mindestens ein Medikament off-label erhielten.
Die Pharmakokinetik unterscheidet sich bei Kindern generell und passt sich erst im Laufe der Entwicklung an die Erwachsenen an. Bei Früh- und Neugeborenen sind diese Unterschiede besonders ausgeprägt und verändern sich stetig. Nahezu alle pharmakokinetischen Prozesse - Absorption, Distribution, Metabolisierung und Elimination - sind betroffen.
Neugeborene werden je nach Gestationsalter in frühgeborene (Geburt < 36 vollendete SSW), termingeborene (Geburt 36 bis 42 vollendete SSW) und übertragene (Geburt > 42 vollendete SSW) Neugeborene eingeteilt. Frühgeborene sind eine besonders vulnerable Patientengruppe, die aufgrund diverser Komplikationen spezielle Therapien benötigt.
Die verminderte Magensäureproduktion von Neugeborenen führt zu einem erhöhten gastralen pH-Wert, was die Resorption schwach saurer Wirkstoffe beeinflusst. Medikamente werden aufgrund der verzögerten Magenentleerung generell langsamer resorbiert.
Die Hautbarriere ist bei Neugeborenen, insbesondere bei Frühgeborenen, noch nicht ausgereift, was zu einer deutlich gesteigerten perkutanen Wirkstoffaufnahme führt.
Die Verteilungsräume unterscheiden sich von denen Erwachsener. Das höhere Körperwasser beeinflusst das Verteilungsvolumen hydrophiler und lipophiler Arzneistoffe.
Neugeborene weisen eine erheblich reduzierte Enzymexpression der am Phase-I- und Phase-II-Metabolismus beteiligten Enzyme auf. Dies ist ausschlaggebend für die Metabolisierung und erfordert Dosisanpassungen.
Auch in der Pharmakodynamik können sich Früh- und Neugeborene von älteren Kindern und Erwachsenen unterscheiden, was zu verstärkten, abgeschwächten oder unvorhersehbaren Arzneimittelwirkungen führen kann.
Aufgrund der sich rasch verändernden Stoffwechsellage, der unreifen Enzymexpression und großer interindividueller Unterschiede spielt das Therapeutische Drug Monitoring (TDM) eine wichtige Rolle bei Früh- und Neugeborenen. TDM bezeichnet die individuell angepasste Dosierung von Arzneistoffen unter Kontrolle der Wirkstoffkonzentration im Blut.
Medizinische Vorsorgeuntersuchungen und Screening
Die Kindervorsorgeuntersuchungen (U-Untersuchungen) zielen darauf ab, Entwicklungsstörungen, chronische Krankheiten oder gesundheitliche Risiken frühzeitig zu erkennen. Der APGAR-Score wird unmittelbar nach der Geburt zur Beurteilung der lebenswichtigen Funktionen erhoben.
Die erste Untersuchung (U1) dient der Feststellung von Geburtstraumata und angeborenen Fehlbildungen. Zwischen dem 3. und 10. Lebenstag steht die U2-Untersuchung an, bei der unter anderem eine Vitamin-K- und Vitamin-D-Prophylaxe erfolgt und das Neugeborene ausführlicher auf angeborene Erkrankungen untersucht wird.
Die U-Untersuchungen erstrecken sich von der Geburt bis zum 6. Lebensjahr (U1 bis U9). Eine Evaluation aus dem Jahr 2024 zur Umsetzung dieser Untersuchungen basierte auf Daten von über 43.000 Untersuchungen.
Die Stuhlfarbkarte zur Erkennung einer Gallengangatresie soll künftig verbindlich ins U-Heft aufgenommen werden. Die meisten Sehtests werden gemäß Richtlinie ausgeführt.
Ebenfalls in den ersten Lebenstagen erfolgt parallel zur U2-Untersuchung ein erweitertes Neugeborenen-Screening, mit dem angeborene Stoffwechselerkrankungen und Endokrinopathien frühzeitig erkannt werden sollen. Hierzu zählen Hypothyreose, Phenylketonurie und spinale Muskelatrophie. Für die Untersuchung wird dem Neugeborenen Blut entnommen.
Die geringe Plazentagängigkeit von Vitamin K führt zu niedrigen Plasmaspiegeln bei Neugeborenen, was die Hämostase beeinträchtigt. Zur Prophylaxe einer Vitamin-K-Mangel-Blutung (VKMB) wird bei Neugeborenen standardmäßig Vitamin K oral substituiert.
Da eine direkte Sonnenexposition bei Neugeborenen und Säuglingen vermieden werden soll und Muttermilch nur geringe Mengen Vitamin D enthält, ist eine orale Substitution von Vitamin D üblich.
Zur Kariesprophylaxe stehen Kombinationspräparate aus Vitamin D und Fluorid zur Verfügung.
Häufige Komplikationen und Behandlungsansätze bei Frühgeborenen
Als Frühgeborenes wird ein Neugeborenes bezeichnet, das vor Vollendung von 36 Schwangerschaftswochen geboren wird. Frühgeborene sind eine besonders vulnerable Patientengruppe und benötigen aufgrund diverser Komplikationen häufig spezielle Therapien.
Atemwegserkrankungen
Das Atemnotsyndrom (Surfactant-Mangel-Syndrom), das mit einer Prävalenz von bis zu 90 Prozent auftritt, ist die Folge eines Surfactant-Mangels aufgrund von Lungenunreife. Bei einem Mangel an oberflächenstabilisierendem Surfactant kollabieren die Alveolen, was zu einer Funktionsstörung der Lunge führt. Typische Symptome sind Tachypnoe und Dyspnoe.
Weitere häufige respiratorische Komplikationen sind idiopathische Apnoen, die mit dem bronchodilatierenden Methylxanthin Coffeincitrat behandelt werden, welches Theophyllin als Standard abgelöst hat.
Kardiovaskuläre Komplikationen
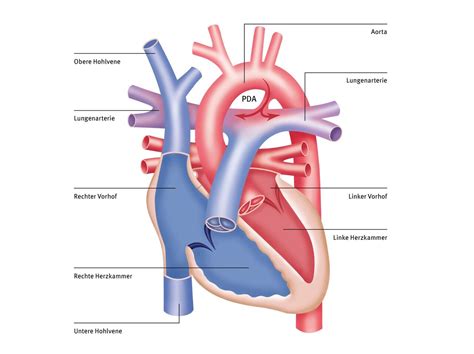
Der Ductus arteriosus (Ductus arteriosus Botalli, DAB) ist ein Shunt im fetalen Blutkreislauf. Bei Frühgeborenen kann es zu einem pathologischen Fortbestehen des Shunts nach der Geburt kommen (persistierender Ductus arteriosus, PDA). Symptome einer Herzinsuffizienz und ein erhöhter Wassergehalt in der Lunge sind die Folge. Der PDA kann medikamentös, chirurgisch oder katheterinterventionell verschlossen werden. Grundlage der medikamentösen Therapie ist die Hemmung der Prostaglandin-Synthese.
Gastrointestinale Komplikationen
Eine der gefürchtetsten gastrointestinalen Notfallsituationen ist die nekrotisierende Enterokolitis (NEK). Bei einer Häufigkeit von 5 bis 7 Prozent aller Frühgeborenen unter 1500 g ist sie mit einer Letalität von 10 bis 50 Prozent die häufigste Todesursache bei vor der 29. SSW geborenen Babys. Die NEK wird hauptsächlich symptomatisch therapiert und mit Breitband-Antibiotika behandelt.
Schmerztherapie
Operationen, Arzneimittelanwendung und Infektionen sind häufige Ursachen von Schmerzen bei Neugeborenen. Zur Behandlung von schwachen bis mittelstarken Schmerzen und Fieber stehen Paracetamol und Ibuprofen zur Verfügung. Ibuprofen ist zur Analgesie erst ab dem dritten Lebensmonat zugelassen, Paracetamol ab Geburt. Erste Wahl bei starken Schmerzen sind Opioide wie Morphin und Fentanyl.
Zur lokalen Analgesie bei oberflächlichen Eingriffen stehen Dermatika mit der Wirkstoffkombination Lidocain/Prilocain zur Verfügung. Bei Frühgeborenen sollte diese Kombination jedoch aufgrund des Risikos erhöhter Methämoglobin-Werte nicht angewendet werden.
Infektionserkrankungen
Aufgrund ihres unreifen Immunsystems sind Früh- und Neugeborene besonders anfällig für schwere bakterielle Infekte. Die neonatale Sepsis (Neugeborenen-Sepsis) ist eine systemische, meist bakterielle Infektion während der Neugeborenen-Phase. Abhängig vom Zeitpunkt der Manifestation unterscheidet man die Early-Onset- (EOS) und die Late-Onset-Sepsis (LOS).
Bei klinischem Verdacht auf eine neonatale Sepsis muss unverzüglich eine antibiotische Therapie gestartet werden. Typisch ist eine Kombination aus Aminopenicillin mit Aminoglykosid, in schweren Fällen ergänzt durch ein Cephalosporin der dritten Generation.
Ebenfalls kritisch sind Harnwegsinfektionen (HWI), die zu den häufigsten bakteriellen Infektionen von Neugeborenen gehören. Zu den klinischen Symptomen zählen Erbrechen, Trinkschwäche, Gewichtsverlust und Ikterus.
Sepsis erkennen: Krankheitszeichen, Diagnose & Behandlung bei einer Blutvergiftung
tags: #theophyllin #dosierung #fruhgeborene