Die enzymatische Katalyse ist ein fundamentaler Prozess in lebenden Organismen, der die Geschwindigkeit chemischer Reaktionen in Lebewesen deutlich erhöht. Enzyme wirken als Katalysatoren, die ohne Verbrauch oder permanente Veränderung die Umwandlung von Substraten in Produkte ermöglichen. Sie sind essenziell für nahezu alle biochemischen Prozesse, von der Verdauung bis zur DNA-Replikation.
Was ist enzymatische Katalyse?
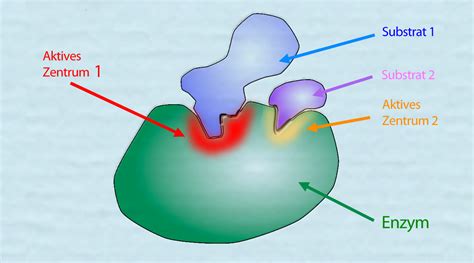
Enzymatische Katalyse bezieht sich auf den Prozess, bei dem ein Enzym die Umwandlung von Substraten (Ausgangsstoffen) in Produkte beschleunigt, ohne dabei selbst verbraucht zu werden. Diese spezialisierten Proteine sind fähig, die Aktivierungsenergie, die notwendig ist, um eine chemische Reaktion zu starten, signifikant zu reduzieren, wodurch die Reaktionsgeschwindigkeit erhöht wird.
Der Ablauf einer enzymatischen Reaktion beginnt mit der Bindung eines Substrats an das aktive Zentrum eines Enzyms. Das Schlüssel-Schloss-Prinzip erklärt die spezifische Bindung zwischen Enzym und Substrat, wobei die dreidimensionale Struktur des aktiven Zentrums genau auf die Form des Substrats abgestimmt ist. Im Verlauf der enzymatischen Katalyse wird die Aktivierungsenergie der Reaktion deutlich herabgesetzt. Dies geschieht durch verschiedene Mechanismen wie räumliche Ausrichtung des Substrats, Einführung von Spannungen oder Ladungsverteilungen.
Grundlagen der Enzymkinetik
Die Enzymkinetik ist ein wichtiger Bereich, der sich mit der Geschwindigkeit enzymatischer Reaktionen und den dabei beteiligten Faktoren beschäftigt. Um die Funktionsweise von Enzymen und ihre Effizienz in biologischen Prozessen zu verstehen, ist es entscheidend, einige grundlegende Konzepte zu kennen:
- Substratsättigung: Ein Zustand, bei dem die Erhöhung der Substratkonzentration keine Steigerung der Reaktionsgeschwindigkeit zur Folge hat, weil alle verfügbaren Enzymmoleküle bereits mit Substrat gesättigt sind.
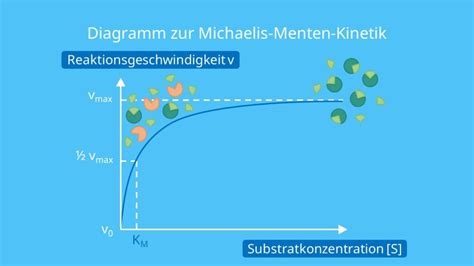
- Michaelis-Menten-Kinetik: Ein Modell, das beschreibt, wie die Reaktionsgeschwindigkeit von der Konzentration des Substrats und Enzyms abhängt. Die Michaelis-Menten-Konstante (Km) ist ein Maß für die Affinität des Enzyms zum Substrat.
Beispiel für Substratsättigung: Stelle dir vor, du füllst ein Wasserglas mit einem kleinen Trichter. Zuerst füllt sich das Glas schnell, aber sobald das Wasser im Trichter den schmalen Hals erreicht, kann es nicht schneller ins Glas fließen, egal wie viel Wasser du oben hinzufügst. In diesem Szenario ist der Trichter das "Enzym", das Wasser das "Substrat" und das Glas die "Reaktionsgeschwindigkeit". Ähnlich erreicht eine enzymatische Reaktion einen Punkt, an dem mehr Substrat die Reaktionsgeschwindigkeit nicht weiter erhöhen kann, weil alle Enzyme besetzt sind.
Faktoren, die die Enzymaktivität beeinflussen
Um die Effizienz von Enzymen in biologischen Systemen zu maximieren, haben sich verschiedene Mechanismen entwickelt, die die Aktivität von Enzymen präzise steuern. Diese umfassen:
- Temperaturoptimum: Jedes Enzym hat eine spezifische Temperatur, bei der es am aktivsten ist. Bei niedrigen Temperaturen ist die Aktivität gering, sie steigt mit zunehmender Temperatur bis zum Optimum an und fällt dann bei zu hohen Temperaturen aufgrund der Denaturierung des Proteins steil ab. Das Temperaturoptimum für menschliche Enzyme liegt typischerweise bei etwa 37°C.
- pH-Wert-Abhängigkeit: Ähnlich wie bei der Temperatur hat jedes Enzym einen optimalen pH-Bereich, in dem es am effektivsten arbeitet. Abweichungen vom optimalen pH-Wert können die Ladung von Aminosäureresten im aktiven Zentrum verändern und somit die Aktivität beeinträchtigen. Verdauungsenzyme wie Pepsin im Magen benötigen beispielsweise einen sauren pH-Wert, während Enzyme im Dünndarm eher im basischen Bereich optimal arbeiten.
- Substratkonzentration: Bei zunehmender Substratkonzentration steigt die Reaktionsgeschwindigkeit zunächst linear an. Sobald jedoch alle Enzymmoleküle mit Substrat besetzt sind (Substratsättigung), erreicht die Geschwindigkeit ihr Maximum (Vmax) und steigt nicht weiter an, auch wenn mehr Substrat hinzugefügt wird.
Die Beeinflussung der Enzymaktivität durch pH-Wert und Temperatur sind fundamentale Prozesse in biologischen Systemen. Enzyme zeigen eine charakteristische Abhängigkeit von der Wasserstoffionenkonzentration ihrer Umgebung, wobei jedes Enzym sein spezifisches pH-Optimum besitzt. Die Abhängigkeit der Enzymaktivität vom pH-Wert Experiment zeigt, dass Verdauungsenzyme unterschiedliche pH-Optima aufweisen.
Coenzyme und Cofaktoren
Coenzyme sind essentielle Helfer der enzymatischen Katalyse. Im Gegensatz zu Enzymen sind sie kleine organische Moleküle, die nur lose mit dem Apoenzym (dem reinen Proteinteil des Enzyms) verbunden sind. Sie fungieren als Reaktionspartner und transportieren beispielsweise chemische Gruppen oder Elektronen. Beispiele für Coenzyme sind NAD+, FAD und ATP.
Der Unterschied zwischen Enzym und Coenzym liegt in ihrer Struktur und Rolle: Während Enzyme große Proteinmoleküle sind, die die Reaktion steuern, sind Coenzyme kleine Moleküle, die als Reaktionspartner fungieren. Die prosthetische Gruppe ist im Gegensatz zum Coenzym dauerhaft mit dem Enzym verbunden.
Der Coenzym-Cofaktor-Unterschied ist bedeutsam für das Verständnis enzymatischer Prozesse. Während Coenzyme organische Moleküle sind, können Cofaktoren auch anorganischer Natur sein, wie z.B. Metallionen (Eisen, Zink, Magnesium), die für die Stabilität oder als Teil des aktiven Zentrums wichtig sind. Enzyme, die Metallionen benötigen, werden als Metalloenzyme bezeichnet.
Mechanismen der Enzymhemmung
Die enzymatische Katalyse kann durch verschiedene Mechanismen gehemmt werden. Diese Hemmung ist ein wichtiger Mechanismus zur Regulation der enzymatischen Aktivität im Körper und spielt auch eine Rolle bei der Wirkungsweise von Medikamenten.
- Kompetitive Hemmung: Hierbei konkurriert ein Inhibitor mit dem Substrat um die Bindung an das aktive Zentrum des Enzyms. Wenn der Inhibitor bindet, kann das Substrat nicht binden und die Reaktion wird verlangsamt oder gestoppt. Diese Hemmung ist oft reversibel, indem die Substratkonzentration erhöht wird.
- Non-kompetitive Hemmung: Bei dieser Form bindet der Hemmstoff an eine andere Stelle des Enzyms (allosterisches Zentrum) und verändert dadurch dessen Struktur so, dass das aktive Zentrum nicht mehr optimal mit dem Substrat interagieren kann. Die Bindung des Inhibitors beeinflusst die Aktivität, aber nicht die Bindung des Substrats.
- Unkompetitive Hemmung: Hier bindet der Hemmstoff nur an den Enzym-Substrat-Komplex und verhindert so die Umsetzung des Substrats.
- Irreversible Hemmung: Ein Inhibitor geht eine dauerhafte, kovalente Bindung mit dem Enzym ein, wodurch dieses permanent inaktiviert wird. Penicillin ist ein Beispiel für einen irreversiblen Inhibitor.
Die pharmazeutische Industrie nutzt das Prinzip der Enzymhemmung, um Medikamente zu entwickeln, die gezielt spezifische Enzyme im Körper hemmen. Statine, die den Cholesterinspiegel senken, hemmen beispielsweise kompetitiv ein Schlüsselenzym der Cholesterinbiosynthese.
Regulation der Enzymaktivität
Enzyme wirken im lebenden Organismus in einem komplexen Geflecht von Stoffwechselwegen zusammen. Um sich schwankenden inneren und äußeren Bedingungen optimal anpassen zu können, ist eine feine Regulation und Kontrolle des Stoffwechsels und der zugrundeliegenden Enzyme nötig.
- Allosterische Regulation: Hierbei binden Effektormoleküle (nicht Substratmoleküle) an spezielle regulatorische Zentren des Enzyms (allosterische Zentren) und beeinflussen dessen Aktivität. Dies ermöglicht eine feine Abstimmung der Enzymaktivität und ist eng mit der Kooperativität mehrerer Bindungsstellen in einem Enzym verbunden.
- Endprodukthemmung (Feedback-Hemmung): Das Endprodukt einer Reaktionskette wirkt als allosterischer Inhibitor auf das Enzym am Anfang dieser Kette. Dies verhindert eine übermäßige Produktion des Endprodukts.
- Kovalente Modifikation: Eine häufige Form der Stoffwechselkontrolle ist die kovalente Modifikation von Enzymen, insbesondere die Phosphorylierung. Dabei wird eine Phosphatgruppe an das Enzym angehängt, was dessen Aktivität ein- oder ausschalten kann, ähnlich einem molekularen Schalter.
- Proteolytische Spaltung: Manche Enzyme werden als inaktive Vorstufen (Zymogene) synthetisiert und erst durch spezifische proteolytische Spaltung aktiviert. Dies ist wichtig für Enzyme, die potenziell schädlich sein könnten, wenn sie ständig aktiv wären, wie z.B. Verdauungsenzyme.
Der katalytische Zyklus eines Enzyms
Der katalytische Zyklus eines Enzyms beschreibt die wiederkehrenden Schritte, die ein Enzym bei der Katalyse einer Reaktion durchläuft:
- Bindung des Substrats: Das Substrat (S) bindet an das aktive Zentrum des Enzyms (E), wodurch ein Enzym-Substrat-Komplex ([ES]) gebildet wird. Dies kann durch das Schlüssel-Schloss-Prinzip oder das flexiblere Induced-Fit-Modell erklärt werden, bei dem sich das aktive Zentrum nach der Bindung des Substrats anpasst.
- Umwandlung des Substrats: Im Enzym-Substrat-Komplex wird das Substrat chemisch umgewandelt, wobei die Aktivierungsenergie durch die Stabilisierung des Übergangszustandes herabgesetzt wird.
- Freisetzung des Produkts: Das umgewandelte Substrat, nun das Produkt (P), wird aus dem aktiven Zentrum des Enzyms freigesetzt.
- Regeneration des Enzyms: Das Enzym (E) liegt nach der Freisetzung des Produkts wieder in seiner ursprünglichen Form vor und ist bereit, ein neues Substratmolekül zu binden und den Zyklus erneut zu durchlaufen.
Dieser Zyklus wiederholt sich kontinuierlich, solange Substrat vorhanden ist und die Bedingungen optimal sind.
Enzyme
Beispiele für enzymatische Katalysen
Enzymatische Katalyse in der Chemie
In der chemischen Industrie werden Enzyme zunehmend genutzt, um nachhaltige Prozesse zu entwickeln. Diese biokatalytischen Methoden bieten zahlreiche Vorteile gegenüber traditionellen chemischen Katalysatoren, darunter eine höhere Spezifität, die Vermeidung von toxischen Metallkatalysatoren und die Möglichkeit, Reaktionen unter umweltfreundlichen Bedingungen durchzuführen.
Beispiel: Die Produktion von Biodiesel durch die Umesterung von Pflanzenölen ist ein typisches Beispiel für enzymatische Katalyse in der Chemie. Hierbei wird das Enzym Lipase verwendet, um die Umesterungsreaktion zwischen Pflanzenöl und einem Alkohol wie Methanol zu katalysieren, wodurch Biodiesel entsteht. Dieser Prozess verläuft bei relativ niedrigen Temperaturen und unter Erhaltung der Umwelt.
Enzymatische Katalyse bei der Fotosynthese
Die Fotosynthese ist ein weiteres eindrucksvolles Beispiel für die Wirkung enzymatischer Katalysen. Sie ist der Prozess, durch den Pflanzen, Algen und einige Bakterien Lichtenergie in chemische Energie umwandeln, um Kohlendioxid und Wasser in Glucose und Sauerstoff zu verwandeln.
Schlüsselenzym: Ein Schlüsselenzym in diesem Prozess ist die Ribulose-1,5-bisphosphat-Carboxylase/Oxygenase, allgemein bekannt als Rubisco. Rubisco katalysiert den ersten bedeutenden Schritt der Kohlenstofffixierung im Calvin-Zyklus, einen Prozess, der atmosphärisches CO2 in organische Kohlenstoffverbindungen umwandelt.
Ein Beispiel für den Einfluss von Enzymen bei der Fotosynthese ist der Prozess der NADPH-Produktion, ein entscheidender Schritt bei der Umwandlung von Lichtenergie in chemische Energie. Die betrachteten Enzyme ermöglichen die Umwandlung von NADP+ und H+ in NADPH, eine für den Calvin-Zyklus unerlässliche Reduktionsäquivalente.
Beispiele für den menschlichen Stoffwechsel
Enzyme sind für praktisch jeden Prozess innerhalb lebender Organismen beteiligt. Von der Verdauung von Nahrungsmitteln über die Replikation von DNA bis hin zur Energiegewinnung durch zelluläre Atmung, ermöglichen Enzyme diese lebenswichtigen Vorgänge.
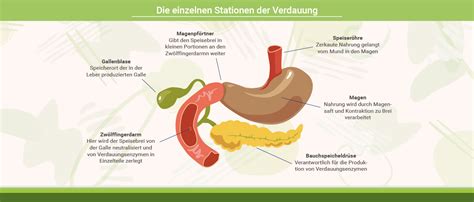
- Verdauungsenzyme: Amylasen im Speichel und Dünndarm spalten Stärke in kleinere Zucker. Lipasen im Dünndarm zerlegen Fette. Proteasen wie Pepsin im Magen und Trypsin im Dünndarm spalten Proteine in Aminosäuren.
- Lactase: Dieses Enzym spaltet den Milchzucker Laktose in die Einfachzucker Glucose und Galactose. Ein Mangel an Lactase führt zu Laktoseintoleranz.
- Katalase: Dieses Enzym kommt in vielen Zellen vor und wandelt das potenziell schädliche Wasserstoffperoxid (H2O2) in harmloses Wasser und Sauerstoff um.
tags: #katalytischer #zyklus #eines #enzyms