Die Entstehung der Gliedmaßen und die frühe Knochenentwicklung
Während der 4. Schwangerschaftswoche bilden sich an den Seiten des sich entwickelnden Embryos Gliedmaßenknospen. Die Spitzen dieser Knospen kondensieren zum apikalen ektodermalen Kamm (AER). Der AER setzt die Verlängerung der Gliedmaßenknospen fort und behält deren Wachstum bei, indem er kontinuierlich den Fibroblasten-Wachstumsfaktor 8 (FGF8) produziert.
Wenn der AER vom Körper wegwächst, differenzieren sich die Gewebe. Arterien dringen in zentrale und periphere Bereiche ein, wodurch primäre und sekundäre Ossifikationszentren entstehen. Die Knochenentwicklung und Ossifikation ist abgeschlossen, wenn sich diese Zentren treffen und die Epiphysenfuge nicht mehr vorhanden ist. Jede der Gliedmaßen nimmt muskuläre Anteile der Myotome mit sich, welche aus Somiten entstehen, und erhält eine eigene nervale Innervation, wodurch Dermatome entstehen.
Die Rolle der Somiten und des Myotoms bei der Muskelentwicklung
Die Somiten, die aus dem Neuralrohr hervorgehen, sind segmentale Zellpakete, die eine entscheidende Rolle bei der Entwicklung des Skeletts und der Muskulatur spielen. Sie spalten sich in eine dorsale Region, das Epimer, das zur intrinsischen Rückenmuskulatur wird, und eine ventrale Region, das Hypomer, das zu den Muskeln der Körperwand und der Gliedmaßen wird.
Wenn das Hypomer in die Gliedmaßenknospen wandert, spaltet es sich in dorsale und ventrale Muskelmassen auf, die zu Extensoren bzw. Flexoren werden. Die Muskulatur der oberen Gliedmaßen entsteht aus Somiten, die C4-C8, T1-T2 entsprechen. Diese führen zu posterioren und anterioren Anteilen der Muskulatur der oberen Extremität. Beugemuskeln entstehen aus den anterioren Anteilen dieser Somiten, während die Streckmuskeln aus den posterioren Anteilen hervorgehen.
Ossifikation: Von Knorpel zu Knochen
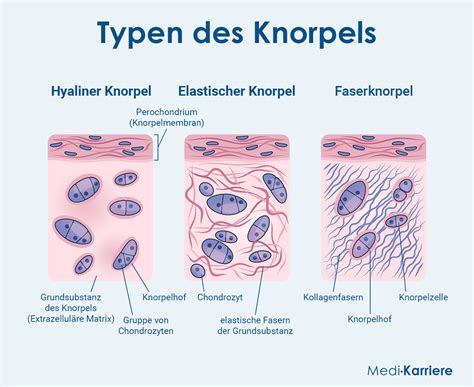
Knorpel entwickelt sich aus undifferenziertem mesenchymalem Gewebe und wird durch enchondrale Ossifikation zu Knochen. Das primäre Ossifikationszentrum wird durch Arterien geschaffen, die in die Mitte des Knorpels eindringen. Ein sekundäres Ossifikationszentrum wird durch Arterien geschaffen, die in die Knochenextremitäten eindringen. Die beiden Ossifikationszentren werden durch die Epiphysenfuge getrennt. Die vollständige Knochenentwicklung und das Schließen der Epiphysenfugen sind in der Regel erst Anfang 20. Lebensjahre abgeschlossen.
Genetische Regulation der Skelettentwicklung
HOX-haltige Gene regulieren mehrere Aspekte des Zellwachstums und der Zelldifferenzierung. Diese Gene sind kranial-kaudal sequentiell angeordnet und bestimmen das Gesamtmuster und die Form des sich entwickelnden Embryos. Mutationen in diesen Genen können die Position und Entwicklung von Gliedmaßen beeinflussen. Die Expression von SHH (Sonic Hedgehog) bestimmt die korrekte anteroposteriore Ausrichtung der Gliedmaßen und beeinflusst somit die Knochenentwicklung und Ossifikation.
Ursprung der Skelettzellen: Ein differenzierter Prozess
Bei Wirbeltieren entsteht das Skelett verschiedener Körperregionen aus unterschiedlichen Vorläuferzellen. Forschende der Universität Basel haben entdeckt, dass sich diese Skelettzellen nicht nur in ihrer Herkunft unterscheiden, sondern auch in ihrer Genregulation. Dies könnte ein Schlüssel zur evolutiven Erfolgsgeschichte der Wirbeltiere sein.
Drei Bauteams mit eigenen Bauplänen
Das Skelett stabilisiert als inneres Gerüst den Körper und bildet schützende Hüllen um wichtige Organe. Trotz ähnlicher Struktur ist Knochen nicht gleich Knochen: Die verschiedenen Teile des Skeletts entstehen im Laufe der Embryonalentwicklung aus drei unterschiedlichen Gruppen von Vorläuferzellen, die jeweils eigene Steuerproteine produzieren und ein eigenes Entwicklungsprogramm durchlaufen.
- Ein Typ von Vorläuferzellen bildet den Schädel und die Gesichtsknochen und entsteht aus Neuralleistenzellen.
- Ein anderer Typ, die somatischen Mesodermzellen, bildet die Wirbelsäule und Rippen. Diese Zellen entstehen am seitlichen Rücken des Embryos und bilden neben Knochen auch Muskeln und Teile der Haut.
- Die dritte Gruppe, die Lateralplatten-Mesodermzellen, bildet das Skelett der Gliedmaßen sowie Teile des Brustkorbs. Diese Zellen befinden sich an den Flanken des Embryos.
Mithilfe von Analysen auf Ebene einzelner Zellen von Hühnerembryos entdeckte ein Forschungsteam, dass diese drei Gruppen unterschiedliche Steuermechanismen verwenden, um das Entwicklungsprogramm hin zu Skelettzellen voranzutreiben. Dies deutet darauf hin, dass es sich um verschiedene Zelltypen handelt, die ein ähnliches Gewebe produzieren.
Die Rolle des Stoffwechsels in der frühen Embryonalentwicklung
Die Glykolyse ist eine evolutionär weit zurückreichende Stoffwechselaktivität, die Glukose in Energie umwandelt und somit grundlegend für Zellwachstum, Teilung und Überleben ist. Forschende haben die Rolle des Stoffwechsels in einzelnen Zellen untersucht, um zu verstehen, wie er ihren Energiezustand beeinflusst.
Glykolyse als Regulator von Zellschicksal und Signalwegen
Studien an Rumpf-artigen Strukturen (in-vitro-stammzellbasierte Embryo-Modelle) haben gezeigt, dass eine blockierte Glykolyse die Bildung von wichtigen Gewebetypen wie Mesoderm (aus dem Muskeln, Knochen oder Blut entstehen) und Endoderm (aus dem Organe wie Leber oder Lunge entstehen) stört. Stattdessen entwickeln sich mehr Zellen zu Ektodermgewebe, aus dem das Nervensystem entsteht. Die Glykolyse unterstützt die Aktivierung wichtiger Signalwege (Wnt, Nodal und Fgf), die die Zellen in Richtung mesodermaler und endodermaler Entwicklung lenken.
Interessanterweise können durch künstliche Verstärkung dieser Signale normale Entscheidungen zum Zellschicksal wiederhergestellt werden, auch ohne dass eine Glykolyse erforderlich ist. Dies unterstreicht die entscheidende Rolle des Stoffwechsels als vorgeschalteter Regulator spezifischer Signalwege, die zelluläre Entscheidungen beeinflussen. Die bioenergetische Funktion der Glykolyse ist wichtig für das Wachstum, während ihre Signalfunktion entscheidend für das Zellschicksal ist. Diese beiden Rollen können entkoppelt werden.
Fehlbildungen der Gliedmaßenentwicklung
Störungen in der komplexen Abfolge von Entwicklungsprozessen können zu verschiedenen Fehlbildungen führen:
- Sirenomelie (Meerjungfrauensyndrom): Eine seltene angeborene Fehlbildung, bei der die Beine miteinander verschmolzen sind. Sie ist gekennzeichnet durch die Fusion der Beine mit Rotation der Wadenbeine und kann mit Anomalien der Wirbelsäule, des Beckens und der Nieren einhergehen. Die Prognose ist oft schlecht.
- Syndaktylie: Bezeichnet das Bestehen von Gewebe zwischen den Fingern oder Zehen. Sie tritt aufgrund des Versagens der Apoptose auf, die für die Trennung der Finger verantwortlich ist.
- Amelie: Das Fehlen eines oder beider Gliedmaßen aufgrund einer Unterbrechung der Entwicklung während der 4. Schwangerschaftswoche.
- Meromelie: Ein Zustand, bei dem ein Teil der Gliedmaße fehlt. Dies tritt aufgrund einer Entwicklungsstörung in der 5. Schwangerschaftswoche auf.
Fortschritte in der Erforschung der frühen Embryonalentwicklung
Die Forschung an menschlichen Embryonen, insbesondere in den frühen Stadien, hat bedeutende Fortschritte gemacht. Die Möglichkeit, menschliche Embryonen bis zum 14. Tag nach der Befruchtung zu untersuchen, unterliegt ethischen und regulatorischen Beschränkungen, die darauf abzielen, die Forschung verantwortungsvoll zu gestalten.
Menschliche Embryonen in der Forschung
Überzählige Embryonen aus Kinderwunschbehandlungen werden in England bis zum 14. Tag für Forschungszwecke genutzt. Diese Forschung zielt darauf ab, die Effizienz der In-vitro-Fertilisation zu verbessern und grundlegende Fragen der menschlichen Entwicklung zu beantworten.
CRISPR-Cas9 und die Untersuchung von Genfunktionen
Die Genschere CRISPR-Cas9 revolutioniert die Molekularbiologie und ermöglicht es Forschern, gezielt Gene in menschlichen Embryonen auszuschalten, um deren Funktion zu untersuchen. So konnte beispielsweise die entscheidende Rolle eines Gens für die Einleitung der Plazentaentwicklung beim Menschen aufgedeckt werden, was sich von Beobachtungen bei Mäusen unterscheidet.
Stammzellbasierte Embryo-Modelle
Gastruloide und rumpfartige Strukturen, die aus embryonalen Stammzellen gezüchtet werden, dienen als Modelle zur Untersuchung der frühen Embryonalentwicklung. Diese Modelle erlauben es, Prozesse zu untersuchen, die sich normalerweise im Uterus der Mutter verbergen, und können zur Erforschung von Entwicklungsdefekten oder zur Testung von Medikamentenwirkungen eingesetzt werden.
Die 14-Tage-Regel
Die 14-Tage-Regel, die die maximale Kultivierungsdauer menschlicher Embryonen für Forschungszwecke festlegt, wurde auf Basis einer politischen und praktischen Einigung etabliert. Sie markiert den Zeitpunkt, ab dem sich der Primitivstreifen bildet und die Anlage der Wirbelsäule beginnt.
Der Zellatlas der Skelettentwicklung
Ein Forschungsteam hat erstmals bis auf die einzelnen Zellen genau entschlüsselt, wie das Skelett eines menschlichen Embryos entsteht und wächst. Durch die Kartierung der Gene und ihrer Aktivität in den Zellen des sich entwickelnden Skeletts und Schädels wurde die erste „Blaupause“ der menschlichen Skelettbildung erstellt.
Entstehung von Knochen: Knorpel als Wegweiser und direkte Bildung
Die Bildung der menschlichen Knochen beginnt etwa sechs bis acht Wochen nach der Befruchtung. In den Gliedmaßen dienen zunächst Knorpelzellen als „Wegweiser“ und Gerüst für die entstehenden Knochen. Beim Schädel des ungeborenen Kindes verläuft die Entwicklung anders: Für das Schädeldach bildet sich kein vorläufiges Gerüst aus Knorpelzellen. Stattdessen vermehren sich knochenbildende Zellen direkt in der Membranhülle des kindlichen Schädels.
Einfluss von Medikamenten auf die Skelettentwicklung
Die Forschung hat auch untersucht, wie gängige Medikamente die Skelettentwicklung des menschlichen Embryos beeinträchtigen können. Diese Erkenntnisse sind wichtig, um die Sicherheit von Medikamenten für Schwangere zu gewährleisten und neue Wirkstoffe spezifischer auf potenzielle Nebenwirkungen zu testen.
Mechanische und elektrische Signale in der Embryonalentwicklung
Neben genetischen und metabolischen Faktoren spielen auch mechanische und elektrische Signale eine Rolle bei der Steuerung der Zellmigration und Gewebebildung während der Embryonalentwicklung. Forschungen deuten darauf hin, dass elektrische Felder die Migration von Zellen, wie beispielsweise den Neuralleistenzellen, während der Entwicklung steuern können.
Elektrotaxis: Zellen folgen elektrischen Feldern
Studien haben gezeigt, dass Zellen der Neuralleiste durch interne elektrische Felder während der Entwicklung geleitet werden. Dieser Prozess, bekannt als Elektrotaxis, ermöglicht es den Zellen, Richtungsinformationen aus elektrischen Feldern zu empfangen und sich entsprechend zu bewegen. Dies ist ein wichtiger Mechanismus, der das Zusammenspiel von Zellen bei der Bildung von Geweben und Organen unterstützt.
Vorsicht, Elektrizität! Napo zeigt die Gefahren
tags: #zellbiologie #knochenentwicklung #embryo