Die lebenswichtige Verbindung zwischen Mutter und Kind
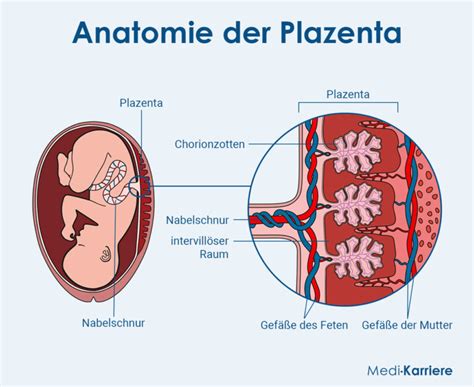
Während der Schwangerschaft erhält das heranwachsende Baby im Mutterleib alle lebensnotwendigen Substanzen über die Nabelschnur. Da das Kind noch nicht selbstständig essen und atmen kann, werden Nährstoffe und Sauerstoff mit dem Blut durch die Nabelschnurvene von der Plazenta zum Kind transportiert. Die Plazenta, auch Mutterkuchen genannt und in der Gebärmutter der Mutter angesiedelt, ist für die Versorgung des Kindes mit Nahrung zuständig.
Besonderheiten des fetalen Blutkreislaufs
Der Blutkreislauf des ungeborenen Kindes unterscheidet sich erheblich von dem eines Neugeborenen, da die Lunge noch nicht aktiv ist. Würde das ungeborene Baby versuchen zu atmen, würde es im Fruchtwasser ertrinken. Um zu verhindern, dass das Blut den Weg durch die Lunge nimmt, existieren zwei spezielle Kurzschlussverbindungen, die dafür sorgen, dass ein Großteil des Blutes direkt in den Körperkreislauf des Babys gelangt.
Das sauerstoff- und nährstoffreiche Blut aus der Nabelschnurvene fließt zunächst in ein Blutgefäß an der Rückseite der Leber und gelangt von dort direkt in die untere Hohlvene. Im rechten Vorhof des Herzens angekommen, wird es fast vollständig durch eine Öffnung in der Vorhofscheidewand, das Foramen ovale, in den linken Vorhof geleitet. Dieser Teil des Blutstroms zielt direkt auf diese Öffnung und vermischt sich nicht mit dem sauerstoffarmen Blut, das gleichzeitig aus der oberen Körperhälfte durch die obere Hohlvene in den rechten Vorhof fließt.
Das sauerstoffreiche Blut aus dem linken Vorhof wird in die linke Herzkammer und von dort in die Hauptschlagader (Aorta) gepumpt. Aus dem Aortenbogen zweigen die Blutgefäße für den Kopf und den oberen Körperbereich ab.
Das sauerstoffarme Blut, das aus der oberen Körperhälfte in den rechten Vorhof gelangt, sowie der verbleibende Anteil des Blutes aus der unteren Hohlvene werden in die rechte Herzkammer und anschließend in den Lungenarterienstamm (Truncus pulmonalis) gepumpt. Da die Lunge des ungeborenen Kindes für den Blutkreislauf noch nicht benötigt wird und entfaltet ist, fließt ein Großteil des Blutes über eine zweite Kurzschlussverbindung, den Ductus arteriosus botalli, direkt in den Aortenbogen.
Der Ductus arteriosus mündet erst nach dem Abzweig der Gefäße für Kopf und Arme in den Aortenbogen ein. Die untere Körperhälfte erhält somit sauerstoffärmeres Blut als die obere. Die Hauptschlagader teilt sich auf Höhe des Bauchnabels in zwei Blutgefäße, die Becken und Beine versorgen. Von der inneren Beckenschlagader zweigen die Nabelarterien ab, die durch die Nabelschnur zur Plazenta zurückführen.
Veränderungen nach der Geburt
Mit dem ersten Atemzug nach der Geburt entfaltet sich die Lunge des Babys und wird voll funktionsfähig. Das Blut strömt nun aus der Lungenarterie durch die Lunge, wird mit Sauerstoff angereichert und fließt über den linken Vorhof und die linke Herzkammer in die Aorta. Dies führt zu einem erhöhten Druck im linken Vorhof im Vergleich zum rechten Vorhof. Infolgedessen verlagert sich die Vorhofscheidewand nach rechts, die Öffnung zwischen den Vorhöfen presst sich zusammen und verschließt sich.
Auch in der Aorta herrscht nach der Geburt ein höherer Druck als im Lungenarterienstamm. Dies kehrt die Flussrichtung des Blutes im Ductus arteriosus botalli um. Bis zum Ende des ersten Lebensjahres sind die Teile der Vorhofscheidewand in der Regel fest miteinander verwachsen.
Die Lunge des Kindes ist im Mutterleib vollständig mit einer Flüssigkeit gefüllt, die von der Lunge selbst produziert wird. Erst kurz vor der Geburt wird diese Flüssigkeit nach und nach abgebaut, und der letzte Rest wird nach der Geburt abgehustet.
Sauerstoffmangel beim Fötus: Risiken und Erkennung
Eine ausreichende Sauerstoffversorgung ist für die ungestörte Entwicklung des Ungeborenen unerlässlich. Besonders in den letzten Schwangerschaftsmonaten, wenn das Baby stark wächst und einen hohen Bedarf an Sauerstoff und Energie hat, kann ein Mangel schnell ungünstige Auswirkungen haben.
Ein Sauerstoffmangel kann dazu führen, dass Kinder vor der Geburt langsamer wachsen als erwartet, was als vermindertes fetales Wachstum bezeichnet wird. Bei extremem Sauerstoffmangel besteht sogar die Gefahr, dass das Kind im Mutterleib stirbt.
Dr. med. Christian Albring, Präsident des Berufsverbandes der Frauenärzte, betont die Wichtigkeit der frühzeitigen Erkennung bedrohlicher Situationen. Wenn eine Frau Wehen hat, insbesondere in den letzten Schwangerschaftswochen, sollte sich die Anzahl der Herzschläge des Babys unter den Wehenkontraktionen und dem damit verbundenen kurzfristig eingeschränkten Blutzufluss nicht verändern. Ein Absinken der Herzfrequenz während oder nach einer Wehe, das sich nur langsam erholt, kann ein Hinweis auf einen Sauerstoffmangel sein.
The Four-Chamber-View of the Fetal Heart - deutsch
Wenn Maßnahmen zur Verbesserung des Zustandes nicht zielführend sind, sollte eine baldige Geburt angestrebt werden. Die Cardiotocographie (CTG), eine Methode zur Überwachung der fetalen Herzfrequenz und der Wehentätigkeit, wird gemäß den Mutterschafts-Richtlinien ab der 26. Schwangerschaftswoche (SSW) bei allen Schwangeren mit Pulsed-Wave-Doppler-Ultraschall durchgeführt. Dabei werden Ultraschallwellen mit sehr geringer Energie verwendet, die als harmlos gelten.
Nach einer neuen Verordnung dürfen Ultraschallanwendungen bei Schwangeren ausschließlich von Frauenärztinnen und -ärzten mit speziellen Qualifikationen durchgeführt werden, sofern eine medizinische Begründung vorliegt. Die Cardiotocographie ist von dieser Verordnung nicht betroffen.
Sauerstofftherapie für Schwangere: Evidenz und Praxis
Manchmal wird empfohlen, dass Schwangere täglich eine kontinuierliche Sauerstofftherapie mit einer Gesichtsmaske erhalten, bis zur Geburt des Kindes. Eine Auswertung von Studien zeigt jedoch, dass es derzeit zu wenig Evidenz dafür gibt, ob diese Therapie das kindliche Wachstum verbessert.
Eine Metaanalyse, die in JAMA Pediatrics veröffentlicht wurde, hat die Ergebnisse von 16 randomisiert kontrollierten Studien (n=2.052) mit Einlingsschwangerschaften ohne Auffälligkeiten verglichen. Dabei wurde die Gabe von Sauerstoff an Mütter während der Geburt mit der Gabe von Raumluft verglichen. Die Forscher bewerteten den pH-Wert des Nabelschnurblutes, die Aufnahmeraten auf der Intensivstation für Neugeborene und die Apgar-Werte. Die Ergebnisse zeigten keinen signifikanten Unterschied im pH-Wert der Nabelschnur-Arterie und keine Verbesserung der Gesundheit der Babys, deren Mütter Sauerstoff erhielten.
Während in den USA jährlich viele schwangere Frauen zusätzlichen Sauerstoff erhalten, ist diese Praxis in Deutschland, zumindest an großen Kliniken, seit über 10 Jahren nicht mehr üblich. Prof. Dr. Sven Kehl vom Perinatal-Zentrum Franken erklärt, dass dies auf dem neuesten wissenschaftlichen Stand basiert. Die Annahme, dass die Gabe von Sauerstoff an die Mutter den Sauerstofftransfer zum Baby erhöht, wird durch die Studie nicht gestützt. Die Autoren empfehlen, die Anwendung von Sauerstoff zu begrenzen, da der Nutzen nicht bewiesen ist.
Fetale Programmierung: Langfristige Auswirkungen von Schwangerschaftsbedingungen
Seit den Beobachtungen von Barker in den 1980er Jahren wird ein Zusammenhang zwischen niedrigem Geburtsgewicht und einem erhöhten Risiko für Herz-Kreislauf-Erkrankungen im Erwachsenenalter diskutiert. Ungünstige Schwangerschaftsbedingungen wie Präeklampsie, mütterliche Adipositas oder Schwangerschaftsdiabetes können den utero-plazentaren Blutfluss reduzieren und zu einer intrauterinen Wachstumsrestriktion (IUGR) führen. Dies erhöht das Risiko für kardiovaskuläre Erkrankungen im Erwachsenenalter bei den Nachkommen. Dieses Phänomen wird als fetale Programmierung bezeichnet, bei der epigenetische Mechanismen eine wichtige Rolle spielen.
Oxidativer Stress wird als potenzieller Mechanismus bei IUGR postuliert. Tiermodelle haben gezeigt, dass die Behandlung mit Antioxidantien wie N-Acetylcystein epigenetische Veränderungen und das intrauterine Wachstum normalisieren kann. Auch Behandlungen mit Substanzen, die antioxidative und NO-stimulierende Wirkungen vereinen, zeigten eine persistierende Blutdrucksenkung bei den Nachkommen.
Studien mit Vitamin C im Rattenmodell der fetalen Programmierung waren wirksam. Allerdings ist die Übertragung der Ergebnisse auf den Menschen aufgrund von Unterschieden in der Entwicklung des Herz-Kreislauf-Systems erschwert.
Eine neuere Studie mit Schafen, die dem Menschen in der fetalen Entwicklung ähnlicher sind, hat die Bedeutung von maternalen Behandlungen mit Antioxidantien zur Prävention einer programmierten Hypertonie bestätigt. Diese Studien sind von hoher Bedeutung für die Translation und stellen eine hoffnungsvolle Präventionsmöglichkeit dar, kardiovaskuläre Erkrankungen bereits im Mutterleib zu bekämpfen.
Dennoch ist eine direkte Übertragung der Ergebnisse auf den Menschen nicht immer möglich. Es muss noch geklärt werden, welches Antioxidans in welcher Dosierung am vielversprechendsten ist. Klinische Studien mit Vitamin C bei IUGR und Präeklampsie waren bisher nicht erfolgreich, insbesondere bei höheren Dosierungen, wie sie in der aktuellen Studie verwendet wurden.
Es ist auch wichtig zu bedenken, dass Tierexperimente oft einen kurzen Beobachtungszeitraum haben und sich auf wenige Organe konzentrieren, was zum Übersehen von Nebenwirkungen führen kann. Ein Beispiel ist die Anwendung von Sildenafil bei IUGR-Modellen, die zwar ermutigende Ergebnisse zeigte, aber zu einer klinischen Studie führte, die wegen einer höheren Inzidenz von pulmonalarterieller Hypertonie des Neugeborenen und erhöhten neonatalen Todesfällen vorzeitig abgebrochen werden musste.
Zusammenfassend bestätigen neuere Studien, dass oxidativer Stress ein wichtiger Mediator der IUGR-programmierten Hypertonie ist und eine maternale Behandlung mit Antioxidantien eine solche Hypertonie verhindern kann. Die Forschung konzentriert sich auf die Entwicklung von Präventionsstrategien, insbesondere für Hochrisikopatientinnen mit schwerer IUGR.
tags: #sauerstoffverbrauch #fotus #mutter